AcuCort AB har utvecklat ISICORT®, ett kortisonbaserat läkemedel som används vid akuta allergiska reaktioner. ISICORT®, en patenterad produkt, är en tunn, snabbupplösande och användarvänlig film som smälter på tungan på 10-15 sekunder med hjälp av munnens saliv. Filmens förpackning är ungefär lika stor som ett visitkort, vilket gör att produkten är smidig att alltid ha med sig. Vidare finns potential för ISICORT® att användas inom fler områden, t.ex. vid viral krupp för småbarn och vid illamående och kräkningar till följd av cellgiftsbehandling. AcuCort är noterat på Spotlight Stock Market sedan 2017.
Press releases
Kommersialisering i fortsatt fokus
ISICORT® har tidigare erhållit godkännande i Sverige och nu pågår även registreringsprocessen för den nordiska marknaden. Ett godkännande i Norden, vilket kan ske under H1-22, innebär att AcuCorts position stärks i de pågående diskussionerna med potentiella kommersiella partners. Rent operativt ser vi att AcuCort utvecklas fortsatt enligt plan. Emellertid har det ekonomiska klimatet under 2022 minst sagt varit kyligt för olönsamma utvecklingsbolag där riskpremierna stigit och investerare skiftat över till bolag med positiva kassaflöden. Vi ser tecken på att denna sektorrotation även påverkat AcuCort, där en ökad riskpremie får en direkt effekt i vår rNPV-modell. Detta innebär en justering av värderingsintervallet vilket nu sträcker sig mellan 2,0 – 6,6 kr med 4,4 (5,4) i ett Base scenario.
- Rapporten i linje med förväntningar
Vid utgången av Q4-21 uppgick kassan till ca 35,9 MSEK, och för de senaste tre rapporterade månaderna (Q4-21) har Bolagets burn rate uppgått till ca -1,3 MSEK per månad. Precis som vi har kommunicerat tidigare kvarhåller vi i våra modeller en förväntan om att AcuCort under kommande kvartal kommer att ha en något högre kapitalförbrukning. Det i sig är helt naturligt med tanke på kommande lansering av ISICORT.
- Nuvarande kassa och kapitalförburkning
Mellan Q3-21 och Q4-21 stärktes AcuCorts kassa med ca 26 MSEK via en företrädesemission samt riktad emission. I vår erfarenhet vet vi att en stärkt kassa för ett mindre läkemedelsbolag likt AcuCort är mycket fördelaktigt i samband med t.ex. att diskussioner förs med potentiella licenstagare. Det skapar nämligen ett bättre förhandlingsutrymme och gör att AcuCort kan agera mindre ”stressat” i förhandlingar, vilket i slutändan kan vara helt avgörande för att ett fördelaktigt avtal ska kunna komma på plats. Med en nuvarande kassa om 35,9 MSEK och en estimerad genomsnittlig burn rate om -1,5 MSEK per månad framgent, skulle det innebära att AcuCort är finansierade tills slutet av 2023, allt annat lika.
- Nytt avtal med kontraktstillverkaren Adhex Pharma
Under Q1-22 meddelade AcuCort att ett nytt avtal tecknats med kontraktstillverkaren Adhex Pharma avseende kommersiell produktion av ISICORT. Detta är en viktig milstolpe för AcuCort då det säkerställer produkt-försörjningen av ISICORT inför lanseringen och minskar således den operationella risken. Vi ser detta som ett robust samarbete med en lämplig partner då Adhex Pharma är specialister inom framställning av tunna munfilmer vilket passar ISICORTs produktprofil.
- Fortsatt attraktiv risk-reward
Med hänsyn till nuvarande börsvärde om ca 75 MSEK och Enterprise Value (EV) om 40 MSEK, samt potentiella värdedrivare framgent, ser vi en fortsatt attraktiv risk-reward i aktien.
Redo att ta nästa kliv
ISICORT® har tidigare erhållit godkännande i Sverige och nu pågår även registreringsprocessen för den nordiska marknaden. Ett godkännande i Norden, vilket kan ske under Q1-22, innebär att AcuCorts position stärks i de pågående diskussionerna med potentiella kommersiella partners. Det, i kombination med en stark finansiell position, är till AcuCorts fördel även vid pågående partnerdialoger på andra prioriterade marknader då det ger AcuCort ett ännu bättre förhandlingsläge. AcuCort tar fortsatt kliv framåt och i samband med Q3-rapporten, samt med hänsyn till den aktuella kapitalstrukturen efter genomförda emissioner, upprepar vi därför vårt värderingsintervall i termer av motiverat riskjusterat bolagsvärde i ett Base scenario. Med hänsyn till de nu 31.2M utestående aktierna, motsvarar det ett nuvärde om 5,4 kr per aktie.
- Rapporten i linje med förväntningar
Vid utgången av Q3-21 uppgick kassan till ca 14,4 MSEK, vilket kan jämföras med ca 17,6 MSEK vid utgången av juni (Q2-21). Under kvartalet uppgick därmed Bolagets burn rate, till -1,1 MSEK/månad, vilket är något lägre än under Q2-21. Precis som vi har kommunicerat tidigare har vi i våra modeller dock räknat med att AcuCort under kommande kvartal kommer att ha en något högre kapitalförbrukning. Det i sig är helt naturligt med tanke på den kommande kommersialiseringen av ISICORT.
- Påfylld kassa
Efter utgången av Q3-21 har AcuCort fyllt på sin kassa med ca 26 MSEK via en företrädesemission samt riktad emission. Med den utgående kassan per den sista september, samt kapitaltillskottet från emissionerna, har AcuCort en stark finansiell position. I vår erfarenhet vet vi att detta för ett mindre läkemedelsbolag likt AcuCort är mycket fördelaktigt i samband med t.ex. att diskussioner förs med potentiella licenstagare. Det skapar nämligen ett bättre förhandlingsutrymme och gör att AcuCort kan agera mindre ”stressat” i förhandlingar, vilket i slutändan kan vara helt avgörande för att ett fördelaktigt avtal ska kunna komma på plats. Med nuvarande finansiell position och ett antagande om en genomsnittlig burn rate om
-1,5 MSEK/månad, skulle det innebära att AcuCort är finansierade tills slutet av 2023.
- Kommersialisering i fortsatt fokus
Vad gäller den kommersiella resan skriver AcuCort att de har växlat upp takten i sina dialoger med potentiella partners i Europa, USA och på utvalda nyckelmarknader som har förmåga att lansera ISICORT på sina respektive lokala marknader. Information kring detta kan komma att utgöra bra värdedrivare i aktien under kommande kvartal.
- Fortsatt attraktiv risk-reward
Med hänsyn till nuvarande Market Cap om ca 87 MSEK och Enterprise Value (EV) om 47 MSEK, samt potentiella väderdrivnare framgent, ser vi en fortsatt attraktiv risk-reward i aktien.
Fortsatt undervärderad läkemedelsaktie
Det stora fokuset framgent är fortsatt hänförligt till arbetet med att lansera ISICORT® på marknaden, vilket inkluderar att allt ska komma på plats så effektivt som möjligt enligt den fastställda planen för att säkerställa en storskalig kommersiell produktion. AcuCort har siktet inställt på flera marknader och lägger nu bl.a. stor vikt vid att anpassa bolagets registreringsansökan för den amerikanska läkemedelsmarknaden i syfte att optimera ett framtida positivt utfall. Även Europa utgör en viktig marknad där AcuCort arbetar med en s.k. Mutual Recognition Process för att registrera ISICORT® på flera marknader inom Europa. I vår mening utvecklas AcuCort helt enligt plan, samtidigt som vi anser att detta inte återspeglas i nuvarande värdering av aktien. I samband med Q2-rapporten upprepar vi därför vårt värderingsintervall, där vi i ett Base scenario ser ett riskjusterat nuvärde om 8 kr (8) per aktie.
- Attraktiv risk-reward i aktien
Parallellt med marknadsarbetet kring ISICORT® pågår aktiva dialoger med olika potentiella licenstagare och samarbetspartners, där AcuCort fokuserar på välrenommerade, resursstarka partners med erfarenhet av allergimarknaden samt med en förmåga att lansera ISICORT® på sin lokala marknad. Eventuell kommunikation kring detta, vilket Analyst Group ser som tänkbart under kommande kvartal i år, kan komma att utgöra en stark värdedrivare i aktien. Med det i åtanke, och med hänsyn till nuvarande bolagsvärde om ca 85 MSEK i skrivande stund, ser vi en fortsatt attraktiv risk-reward i aktien.
- Ökat burn rate i linje med estimat
Vid utgången av Q2-21 uppgick kassan till ca 17,6 MSEK, vilket kan jämföras med ca 21,6 MSEK vid utgången av mars (Q1-21). Under Q2-21 uppgick därmed AcuCorts kapitalförbrukning, s.k. burn rate, till -1,3 MSEK/månad, vilket därmed är något högre än under föregående kvartal (-0,8 MSEK/mån). Precis som vi har kommunicerat tidigare till marknaden har vi i våra modeller räknat med att AcuCort under kommande kvartal kommer att ha en något högre kapitalförbrukning. Det i sig är helt naturligt med tanke på den kommande kommersialiseringen av ISICORT®. Med det sagt, och med tanke på den utgående kassan per den sista juni, anser vi fortsatt att AcuCort har en stark finansiell position. Bolaget har dessutom nyligen flyttat till mer kostnadseffektiva lokaler, vilket förväntas bidra positivt till kommande månaders kassaflöde.
- Upprepar uppsida i ett Base scenario
Vi ser fortsatt positivt på AcuCort som utvecklas i linje med våra förväntningar. Därmed, i samband med Q2-rapporten, väljer vi att behålla vårt tidigare värderingsintervall och upprepar vårt Base scenario där vi ser ett riskjuterat nuvärde per aktie om 8 kr.
Siktet inställt mot marknadslansering
AcuCort verkar göra alla rätt och allt pekar nu på att en lansering av ISICORT, där Sverige blir första marknad, är närstående. Mer än 20 % av jordens befolkning lider av allergi i någon form och andelen drabbade ökar snabbt, något som förväntas kunna bidra till en snabbare försäljningstillväxt av just ISICORT. Parallellt arbetar AcuCort vidare med de regulatoriska processerna i EU och USA. I vår mening utvecklas AcuCort helt enligt plan och med en fortsatt god kostnadskontroll har Bolaget en stark finansiell position. I samband med Q1-rapporten har vi valt att lämna vårt värderingsintervall oförändrat, där vi i ett Base scenario upprepar ett riskjusterat nuvärde om 8 kr (8) per aktie.
- Kostnadskontroll på toppnivå
Under Q1-21 uppgick AcuCorts totala rörelsekostnader till ca 2 MSEK (2,7), motsvarande en minskning om ~25 % mot jämförbart kvartal 2020 samtidigt som det var i linje med föregående kvartal (Q4-20). Vi anser att AcuCort tillhör den kategorin av läkemedelsbolag på de mindre börslistorna som uppvisar högst grad av kostnads-kontroll. Med tanke på det läget som Bolaget befinner sig i, med en närstående kommersialisering, är detta såklart något vi ser positivt på. Samtidigt, till följd av just kommersialiseringen, räknar vi med att AcuCorts totala kostnadsbas kommer att stiga framgent, vilket är naturligt under en sådan fas.
- Marknadslansering och licensavtal runt hörnet
Under H1-21 har AcuCorts team stärkts ytterligare med Louise Harting, som har tidigare erfarenhet från bl.a. Novo Nordisk där hon hade ansvar hänförligt till internationella produktlanseringar inom läkemedelsindustrin – erfarenheter som minst sagt passar väl in i rådande läge för AcuCort. Pusselbitarna för en framgångsrik introduktion av ISICORT på marknaden faller på plats en efter en, parallellt med att diskussioner fortsatt pågår med tänkbara licenstagare och samarbets-parters. Lansering och ett licensavtal bedömer vi skulle utgöra starka värdedrivare i aktien.
- Fortsatt stark finansiell position
AcuCort har under lång tid bevisat sin förmåga att utveckla verksamheten med god kostnadskontroll, något som även blev fallet under Q1-21. Under kommande kvartal räknar vi dock som sagt med att AcuCort kommer ha en något högre kapitalförbrukning, vilket är helt naturligt med tanke på den kommande lanseringen. Likväl, med senast rapporterad kassa om 22 MSEK, anser vi fortsatt att AcuCort har en stark finansiell position.
- Bibehåller vårt värderingsintervall
AcuCort utvecklas in linje med våra förväntningar, varför vi endast gjort mindre justeringar i vår finansiella modell. I samband med Q1-rapport väljer vi därför att lämna värderingsintervallet oförändrat i samtliga tre scenarion Base-, Bull- och Bear.
Kommersialisering och regulatoriskt arbete i fokus
Mer än 20 % av jordens befolkning lider av allergi i någon form och andelen drabbade ökar snabbt. Många drabbas även av svåra reaktioner i situationer där tillgång till t.ex. vatten är begränsad. ISICORT® tillgodoser ett tydligt behov och med ett marknadsgodkännande i Sverige sedan oktober fokuserar AcuCort nu på att kommersialisera produkten. Parallellt arbetar AcuCort vidare med de regulatoriska processerna i EU och USA. I vår mening utvecklas AcuCort helt enligt plan och med en fortsatt god kostnadskontroll har Bolaget en stark finansiell position. I samband med Q4-rapporten har vi valt att lämna vårt värderingsintervall oförändrat, där vi i ett Base scenario ser ett riskjusterat nuvärde om 8 kr per aktie.
- Godkännande för behandling av Covid-19
Under H1-20 uppmärksammades det att dexametason, vilket är den aktiva substansen i AcuCorts produkt ISICORT, kan reducera dödligheten bland personer som insjuknat i Covid-19. Sedan dess har Bolaget fortsatt att följa fördjupningsstudier i frågan, och under februari 2021 beviljade det svenska Läkemedelsverket ISICORT-indikationen för behandling av patienter med Covid-19 som behöver syrgasbehandling. Utöver att fylla en viktig funktion inom vården, kommer detta även väl till hands för AcuCort i samband med de kommande ansökningarna om marknadsgodkännande inom EU och USA.
- Värdedrivande aktiviteter under 2021
Val av försäljningspartner och distributörer, marknadsföringsstrategi, den nationella pris- och subventionsansökan, förberedelser för kommersiell produktion och logistik – alla dessa aktiviteter och tillhörande kommunikation från AcuCort utgör potentiella värdedrivare i aktien under kommande kvartal 2021. Parallellt med kommersialiseringsarbetet av ISICORT i Sverige arbetar AcuCort vidare med att erhålla godkännande inom EU genom den s.k. Mutual Recognition Procedure (MRP). Även arbetet med USA-registrering fortgår, där AcuCort i samråd med FDA har identifierat en regulatorisk strategi för marknadsgodkännande.
- Fortsatt stark finansiell position
AcuCort har under lång tid bevisat sin förmåga att utveckla verksamheten med god kostnadskontroll, något som även blev fallet under Q4-20. Under kommande kvartal räknar vi dock med att AcuCort kommer ha en något högre kapitalförbrukning, vilket är helt naturligt med tanke på den kommande kommersialiseringen. Likväl, med senast rapporterad kassa om 24 MSEK, anser vi fortsatt att AcuCort har en stark finansiell position.
- Bibehåller vårt värderingsintervall
AcuCort utvecklas in linje med våra förväntningar, varför vi endast gjort mindre justeringar i vår finansiella modell. I samband med Q4-rapport väljer vi därför att lämna värderingsintervallet oförändrat i samtliga tre scenarion Base-, Bull- och Bear.
Läkemedelsbolaget som går från klarhet till klarhet
ISICORT® erhöll under oktober marknadsgodkännande från svenska Läkemedelsverket, varpå förberedelser för kommersialiseringsfasen nu pågår för fullt. Parallellt avser AcuCort att ansöka om vidare godkännande inom EU, och har dessutom i samråd med FDA i USA identifierat en regulatorisk strategi för ett godkännande på den amerikanska marknaden. I vår bok går AcuCort från klarhet till klarhet, samtidigt som Bolagets likvida medel utgör en fortsatt trygghet i balansräkningen. Med hänsyn till godkännandet från Läkemedelsverket har vi i samband med Q3-rapporten valt att justera upp vårt värderings-intervall. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om ca 157 MSEK, motsvarande 8 kr (6) per aktie, i ett Base scenario.
- Erhållit godkännande av Läkemedelsverket
Under oktober 2020 stod det klart att Läkemedelsverket i Sverige givit ISICORT marknadsgodkännande, ett besked som vi i vårt Base scenario räknande med skulle komma först mot slutet av Q4-20 men som nu levererades ett par veckor tidigare. Förberedande aktiviteter pågår nu för marknadslansering i Sverige, bl.a. sammanställning av en nationell pris- och subventionsansökan, förberedelser för kommersiell produktion och logistik samt implementering och godkännande av ett uppdaterat kvalitetssystem som möjliggör partihandelstillstånd. Vi kommer följa noga hur detta arbete fortlöper och vad som kan komma att kommuniceras från AcuCort, då nämnda faktorer styr när en aktiv försäljning av ISICORT kan påbörjas i Sverige.
- Pågående diskussioner med samarbetspartners
AcuCort har meddelat att det pågår fortlöpande dialoger med potentiella framtida partners som tillsammans med AcuCort kan ansvara för försäljning och marknadsföring av ISICORT på de lokala marknaderna. Ett eventuellt samarbete skulle kunna utgöra en potentiellt stark värdedrivare i aktien under kommande tolv månader.
- Fortsätter bearbeta EU och USA
AcuCort avser att ansöka vidare om godkännande inom EU genom den s.k. Mutual Recognition Procedure (MRP). AcuCort har även i samråd med FDA identifierat en regulatorisk strategi för ett godkännande i USA. Regulatoriska framgångar inom EU och USA kan ses som ytterligare tänkbara ”triggers” i aktien.
- Höjer vårt värderingsintervall
ISICORT har fått godkänt av Läkemedelsverket och står nu närmare marknaden än någonsin förr, samtidigt som AcuCort för tillfället värderas till omkring 118 MSEK (Market Cap). Med tanke på ISICORT:s produktegenskaper, närheten till marknaden och AcuCorts finansiella ställning idag, kan det argumenteras för att det borde finnas utrymme för högre värderingsnivåer i aktien. I samband med Q3-rapport har vi därför valt att höja vårt värderingsintervall i samtliga tre scenarion Base-, Bull- och Bear.
Marknadsgodkännande kan ligga runt hörnet
AcuCorts produkt ISICORT® skulle kunna närma sig marknadsgodkännande i Sverige mot slutet av 2020 och försäljningen estimeras då påbörjas under 2021. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och nuvarande ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om ca 115 MSEK, motsvarande 6 kr per aktie, i ett Base scenario.
- Fortsätter ta steg mot markandslansering
Under Q2-20 har AcuCort fortsatt lagt ett stort fokus kring att ta fram bra underlag till Läkemedelsverket för ansökan om ett nationellt marknadsgodkännande av ISICORT, där AcuCort enligt plan den 11 augusti 2020 lämnande in svarsdossiern avseende den andra utvärderingsrapporten. AcuCort fortsätter ta steg i rätt riktning och i dagsläget ser Analyst Group det som fortsatt möjligt att ISICORT skulle kunna närma sig ett marknadsgodkännande i Sverige mot slutet av det här året.
- Ny VD rekryterad
Jonas Jönmark tillträdde under augusti som ny VD, han har en MBA-examen från Lunds universitet och över 20 års erfarenhet från ledande befattningar och VD-roller inom läkemedelsindustrin och life science-sektorn. Hans karriär har inkluderat stora internationella läkemedelsföretag, bl.a. Pfizer, Astellas Pharma och Astra Zeneca, samt även mindre startupbolag som Life Science Support och Alteco Medical. Med tanke på Jonas tidigare erfarenheter av internationella produktlanseringar, etablering av sälj- och distributionskanaler, kommersiella partnerskap, prissättnings- och ersättningsförhandlingar med myndigheter samt internationell affärsutveckling, anser vi att rekryteringen är en värdefull beståndsdel i den utvecklingen som ska ta AcuCort till nya nivåer.
- Stabil kassa minskar den finansiella risken
Under H1-20 uppgick AcuCorts operativa kapitalförbrukning, s.k. burn rate, till ca -0,8 MSEK/månad, vilket vi anser är lågt och således något vi ser positivt på. En viktig faktor att ta i beaktande är hur länge nuvarande likviditet räcker till. Med avstamp i den utgående kassan per juni månad, historisk burn rate och en uppskattning kring framtida kapitalbehov, räknar vi med att AcuCort är finansierade en bra bit in i 2021.
- Lämnar vårt värderingsintervall oförändrat
ISICORT står nära marknaden och för tillfället värderas AcuCort till omkring 100 MSEK (Market Cap). Med tanke på ISICORT:s produktegenskaper, närheten till marknaden och AcuCorts finansiella ställning idag, kan det argumenteras för att det borde finnas utrymme för högre värderingsnivåer i aktien.
Fortsätter att ta steg i rätt riktning
AcuCorts produkt ISICORT® skulle kunna närma sig marknadsgodkännande i Sverige mot slutet av 2020 och försäljningen estimeras då påbörjas under 2021. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om ca 115 MSEK, motsvarande 6 kr per aktie, i ett Base scenario.
- Fokus på svarsrapporten till Läkemedelsverket
Under februari erhöll AcuCort den första utvärderingsrapporten från Läkemedelsverket av den nationella ansökan om marknadsgodkännande för ISICORT. Rapporten omfattar både en klinisk del och en kvalitetsdel, med en huvudpart av praktiska frågor rörande kvalitet och tillverkning. Senaste veckorna har AcuCort lagt ett stort fokus på att ta fram en svarslista med goda underlag, där målbilden är att AcuCort ska lämna in sin rapport till Läkemedelsverket den 8 maj. I dagsläget ser Analyst Group det som fortsatt möjligt att ISICORT skulle kunna närma sig ett marknadsgodkännande i Sverige mot slutet av det här året.
- Endast begränsade effekter från Covid-19
I Q1-rapporten skriver AcuCort om hur effekterna av pandemi-utbrottet kan påverka Bolagets situation och/eller utveckling, där bedömningen för närvarande är att påverkan endast är begränsad. I nuläget är AcuCorts samarbete med sin tillverkningspartner och regulatoriska experter av stor vikt, vilka skall ha säkrat en fortlöpande verksamhet med bibehållen kvalitetsnivå.
- Fortsatt goda möjligheter för USA-registrering
AcuCort meddelade i början av året en positiv syn på att utfallet i den andra bioekvivalensstudien för USA inte är ett hinder för att ansöka om marknadsgodkännande av ISICORT på USA-marknaden. Den tidigare tillsatta expertgruppen presenterade bl.a. handlingsalternativ för att möjliggöra registrering och kommersialisering av ISICORT på den amerikanska marknaden. Vad som är extra betryggande är att dessa slutsatser har bekräftats av ytterligare två oberoende expertinstanser i USA och Tyskland.
- Risker kring kapitalbehov och samarbetsavtal
AcuCort genomförde under hösten 2019 en nyemission om ca 41 MSEK, vilken förväntas kunna täcka kapital-behovet en bra bit in i 2021. Däremot kan framtida nyemissioner inte uteslutas, vilket i sig får anses utgöra en riskfaktor. Vidare får även avsaknad av samarbetspartners ses som en potentiell risk. Detta är dock något som AcuCort arbetar intensivt med, där det har kommunicerats att samtal pågår.
Fortsätter att närma sig marknadslansering
AcuCorts produkt ISICORT® skulle kunna närma sig marknadsgodkännande i Sverige mot slutet av 2020 och försäljningen estimeras påbörjas under 2021. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om ca 115 MSEK, motsvarande 6 kr per aktie, i ett Base scenario.
- Fortsatt goda möjligheter för USA-registrering
AcuCort meddelade tidigare i år en positiv syn på att utfallet i den andra bioekvivalensstudien för USA inte är ett hinder för att ansöka om marknadsgodkännande av ISICORT på USA-marknaden. Nyheten var minst sagt välkommen där den tidigare tillsatta expertgruppen bl.a. presenterade handlingsalternativ för att möjliggöra registrering och kommersialisering av ISICORT på den amerikanska marknaden. Det känns även extra betryggande att dessa slutsatser har bekräftats av ytterligare två oberoende expertinstanser i USA och Tyskland.
- Har fått svar från Läkemedelsverket
Under september 2019 lämnade AcuCort in en nationell hybridansökan för marknadsgodkännande av ISICORT till svenska Läkemedelsverket. Under februari 2020 meddelade AcuCort att myndigheten återkommit med den första utvärderingsrapporten, där det bl.a. framgick att ”[…] Det gavs inga formella starka invändningar och den initiala analysen av rapporten och frågelistan tyder inte på några stora stötestenar.” Utfallet är såklart något vi anser är minst sagt positivt.
- Vi behåller vår positiva syn på bolaget
ISICORT är en produkt som verkligen kan hjälpa patienter till en bättre livskvalitet, inom flera olika områden. Produkten står nära marknaden och för tillfället värderas AcuCort till omkring 60 MSEK (Market Cap). Med tanke på ISICORT:s produktegenskaper, närheten till marknaden och AcuCorts finansiella ställning idag, kan det argumenteras för att det borde finnas utrymme för högre värderingsnivåer i aktien.
- Risker kring kapitalbehov och samarbetsavtal
AcuCort har under hösten 2019 genomfört en nyemission om ca 41 MSEK, vilket förväntas kunna täcka kapitalbehovet en bra bit in i 2021. Däremot kan framtida nyemissioner inte uteslutas, vilket i sig får anses utgöra en riskfaktor. Vidare får även avsaknande av samarbetspartners ses som en potentiell risk. Detta är dock något som AcuCort arbetar intensivt med, där det har kommunicerats att samtal pågår.
Kommersialisering inom räckhåll efter fortsatta steg mot godkännande
AcuCorts produkt ISICORT®, som innan namnbyte hette Dexa ODF, väntas nå marknadsgodkännande i Sverige under 2020 och försäljningen estimeras påbörjas tidigt 2021. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 102 MSEK, motsvarande 5,2 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, ISICORT är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flera fördelar jämfört med dagens alternativ. En film är stark nog för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. ISICORTs förpackning är är ungefär lika stor som ett visitkort, vilket gör att det alltid är lättillgängligt.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvudägare, AQILION AB (tidigare P.U.L.S. AB), är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag med ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- Tydlig väg mot kommersialisering
Under 2019 har AcuCort skickat in ansökan till Läkemedelsverket och det innebär att ISICORT kan bli godkänt i Sverige under 2020. Givet ett godkännande kan Bolaget sedan gå vidare genom en så kallad Mutual Recognition Process för att få godkännande i fler EU-länder. Osäkerhet har uppstått kring registreringen av ISICORT i USA på grund av att bioekvivalens inte kunde visas i den andra av två studier. Den första studien har visat bioekvivalens. Givet godkänt läkemedel krävs det att AcuCort sluter avtal med samarbetspartners, för distribution och/eller licensiering, för att kommersialiseringen ska lyckas.
- Risk relaterad till kapitalbehov och samarbetsavtal
Bolaget har genomfört en nyemission om 42,1 MSEK, vilket förväntas täcka kapitalbehovet en bit in i 2021, däremot kan framtida nyemissioner inte uteslutas. Vidare får även avsaknaden av samarbetspartners ses som en risk. Detta är något som Bolaget dock jobbar intensivt med, där de har kommunicerat att samtal pågår.
Kommersialisering närmare efter fortsatta steg mot godkännande
AcuCorts produkt ISICORT®, som innan namnbyte hette Dexa ODF, väntas nå marknadsgodkännande under 2020 och försäljningen estimeras påbörjas tidigt 2021. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 199 MSEK, motsvarande 10,1 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, ISICORT är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flera fördelar jämfört med dagens alternativ. En film är stark nog för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. ISICORTs förpackning är är ungefär lika stor som ett visitkort, vilket gör att det alltid är lättillgängligt.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvudägare, AQILION AB (tidigare P.U.L.S. AB), är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag med ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- Tydlig väg mot kommersialisering
Under 2019 har AcuCort fortsatt tagit viktiga steg mot att få läkemedelsgodkännande i EU och USA. Ansökan väntas skickas in till EU under hösten 2019, vilket kan innebära godkännande under 2020. Även processen i USA fortsätter enligt plan, då godkännande för den andra av två bioekvivalensstudier nyligen fick klartecken att påbörjas. Givet godkänt läkemedel krävs det att AcuCort sluter avtal med samarbetspartners, för distribution och/eller licensiering, för att kommersialiseringen ska lyckas. Bolaget för idag diskussioner med potentiella samarbetspartners men statusen för dessa är okänt.
- Risk relaterad till kapitalbehov och samarbetsavtal
Bolaget genomför en nyemission om 42,1 MSEK, vilket förväntas täcka kapitalbehovet en bit in i 2021, däremot kan framtida nyemissioner inte uteslutas. Vidare får även avsaknaden av samarbetspartners ses som en risk. Detta är något som Bolaget dock jobbar intensivt med, där de har kommunicerat att samtal pågår.
Kommersialisering närmare efter fortsatta steg mot godkännande
AcuCorts produkt ISICORT®, som innan namnbyte hette Dexa ODF, väntas nå marknadsgodkännande under 2020 och försäljningen estimeras påbörjas i slutet av 2020. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 199 MSEK, motsvarande 16,0 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, ISICORT är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flera fördelar jämfört med dagens alternativ. En film är stark nog för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. ISICORTs förpackning är är ungefär lika stor som ett visitkort, vilket gör att det alltid är lättillgängligt.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvudägare, AQILION AB (tidigare P.U.L.S. AB), är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag med ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- Tydlig väg mot kommersialisering
Under 2019 har AcuCort fortsatt tagit viktiga steg mot att få läkemedelsgodkännande i EU och USA. Ansökan väntas skickas in till EU under hösten 2019, vilket kan innebära godkännande under 2020. Även processen i USA fortsätter enligt plan, då godkännande för den andra av två bioekvivalensstudier nyligen fick klartecken att påbörjas. Givet godkänt läkemedel krävs det att AcuCort sluter avtal med samarbetspartners, för distribution och/eller licensiering, för att kommersialiseringen ska lyckas. Bolaget för idag diskussioner med potentiella samarbetspartners men statusen för dessa är okänt.
- Risk relaterad till kapitalbehov och samarbetsavtal
Bolaget har kommunicerat att en ny kapitalanskaffning kommer krävas under 2019, vilken väntas under H2-19. Villkoren är dock i dagsläget okända. Vidare får även avsaknaden av klara samarbetspartners ses som en risk. Detta är något som Bolaget dock jobbar intensivt med, där de har kommunicerat att samtal pågår.
Flertalet potentiella triggers under resterande delen av 2019
AcuCorts produkt Dexa ODF väntas nå marknadsgodkännande under 2020 och försäljningen estimeras påbörjas i slutet av 2020. Dexa ODF har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 199 MSEK, motsvarande 16,0 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, Dexa ODF, är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flertalet fördelar för patienten jämfört med dagens alternativ. En film är tillräckligt stark för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. Dexa ODF förpackas även i en liten försluten förpackning som är ungefär lika stor som ett visitkort, vilket gör att det går att ha med sig produkten i t.ex. plånboken, och alltid kan vara tillgänglig när allergireaktionen inträffar. Patientfördelarna bedöms attraktiva och bidra till ökad försäljning givet en lyckad marknadslansering.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvud-ägare, AQILION AB (tidigare P.U.L.S. AB), är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag med ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- I ett Base scenario värderas AcuCort till ett riskjusterat nuvärde om 16,0 kr per aktie
Bolagets ambition är att använda sig av ett globalt nätverk av samarbetspartners, där samarbeten antingen är distributions- eller licensbaserade. Givet att Bolaget når marknaden estimeras AcuCorts kassaflöden från Dexa ODF till ett riskjusterat nuvärde om 16,0 kr per aktie.
- Risk relaterad till kapitalbehov och samarbetsavtal
Bolaget har kommunicerat att en ny kapitalanskaffning kommer krävas under 2019, som väntas under H2-19 vilket innebär en okänt stor utspädning. Vidare får även avsaknaden av klara samarbetspartners ses som en risk. Detta är något som Bolaget dock jobbar intensivt med, där de har kommunicerat att samtal pågår.
Kommer allt närmare en kommersialisering av allergiläkemedel
AcuCorts produkt Dexa ODF väntas nå marknadsgodkännande under 2020 och försäljningen estimeras påbörjas i slutet av 2020. Dexa ODF har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 195 MSEK, motsvarande 15,7 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, Dexa ODF, är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flertalet fördelar för patienten jämfört med dagens alternativ. En film är tillräckligt stark för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. Dexa ODF förpackas även i en liten försluten förpackning som är ungefär lika stor som ett visitkort, vilket gör att det går att ha med sig produkten i t.ex. plånboken, och alltid kan vara tillgänglig när allergireaktionen inträffar. Patientfördelarna bedöms attraktiva och bidra till ökad försäljning givet en lyckad marknadslansering.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvudägare, AQILION AB (tidigare P.U.L.S. AB), är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag med ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- I ett Base scenario värderas AcuCort till ett riskjusterat nuvärde om 15,7 kr per aktie
Bolagets ambition är att använda sig av ett globalt nätverk av samarbetspartners, där samarbeten antingen är distributions- eller licensbaserade. Givet att Bolaget når marknaden estimeras AcuCorts kassaflöden från Dexa ODF till ett riskjusterat nuvärde om 15,7 kr per aktie.
- Risk relaterad till kapitalbehov och samarbetsavtal
Bolaget har kommunicerat att en ny kapitalanskaffning kommer krävas under 2019, som väntas under H2-19 vilket innebär en okänt stor utspädning. Vidare får även avsaknaden av klara samarbetspartners ses som en risk. Detta är något som Bolaget dock jobbar intensivt med, där de har kommunicerat att samtal pågår.
AcuCorts produkt Dexa ODF väntas nå marknadsgodkännande mot slutet av 2019 och försäljningen påbörjas då under mitten av 2020. Dexa ODF har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 135 MSEK, motsvarande 10,9 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, Dexa ODF, är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flertalet fördelar för patienten jämfört med dagens alternativ. En film är tillräckligt stark för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. Dexa ODF förpackas även i en liten försluten förpackning som är ungefär lika stor som ett visitkort, vilket gör att det går att ha med sig produkten i t.ex. plånboken, och alltid kan vara tillgänglig när allergireaktionen inträffar. Patientfördelarna bedöms attraktiva och bidra till ökad försäljning givet en lyckad marknadslansering.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvudägare, P.U.L.S. AB, är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag, där han har haft ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- I ett Base scenario värderas AcuCort till ett riskjusterat nuvärde om 10,9 kr per aktie
Bolagets ambition är att använda sig av ett globalt nätverk av samarbetspartners, där samarbeten antingen är distributions- eller licensbaserade. Givet att Bolaget når marknaden estimeras AcuCorts kassaflöden från Dexa ODF till ett riskjusterat nuvärde om 10,9 kr per aktie.
- Risk relaterad till kapitalbehov
Då Bolaget nyligen tog in 10,8 MSEK (efter emissions-kostnader) via en företrädesemission är den finansiella risken på kort sikt låg. Däremot bedöms den nuvarande kassan inte räcka för att nå break even, varför Bolaget förväntas behöva genomföra ytterligare en kapitalanskaffning under H2-2019.
AcuCorts produkt Dexa ODF väntas nå marknadsgodkännande mot slutet av 2019 och försäljningen påbörjas då under mitten av 2020. Dexa ODF har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om 123 MSEK, motsvarande 9,8 SEK per aktie, i ett Base scenario.
- Patientfördelar med produkten talar för framtida tillväxt
AcuCorts produkt, Dexa ODF, är en film som läggs på tungan, som sedan löses upp via munnens saliv. Produkten erbjuder flertalet fördelar för patienten jämfört med dagens alternativ. En film är tillräckligt stark för att räcka per allergisk reaktion. Det krävs inget vatten, vilket är av vikt då en akut allergisk reaktion ofta sker vid ett tillfälle då tillgång till just vatten saknas. Dexa ODF förpackas även i en liten försluten förpackning som är ungefär lika stor som ett visitkort, vilket gör att det går att ha med sig produkten i t.ex. plånboken, och alltid kan vara tillgänglig när allergireaktionen inträffar. Patientfördelarna bedöms attraktiva och bidra till ökad försäljning givet en lyckad marknadslansering.
- Kompetent och erfaren ledning och styrelse
AcuCorts VD och styrelse besitter en bred kompetens och erfarenhet från läkemedelsbranschen. Bolagets huvudägare, P.U.L.S. AB, är ett bolag vars affärsmodell är att investera i life science-projekt för att sedan utveckla dessa. Bolagets styrelse består av både medicinkunniga och marknadskunniga människor som har kompetenser och erfarenheter från läkemedelsutveckling samt regulatoriska frågor inom ansökningsprocesser gällande läkemedelsansökningar. Vidare har även VD Mats Lindfors en lång erfarenhet inom branschen från tidigare uppdrag, där han har haft ledande befattningar inom försäljning och marknadsföring från bl.a. HemoCue AB.
- I ett Base scenario värderas AcuCort till ett riskjusterat nuvärde om 9,8 kr per aktie
Bolagets ambition är att använda sig av ett globalt nätverk av samarbetspartners, där samarbeten antingen är distributions- eller licensbaserade. Givet att Bolaget når marknaden estimeras AcuCorts kassaflöden från Dexa ODF till ett riskjusterat nuvärde om 9,8 kr per aktie.
- Risk relaterad till kapitalbehov
Då Bolaget nyligen tog in 10,8 MSEK (efter emissionskostnader) via en företrädesemission är den finansiella risken på kort sikt låg. Däremot bedöms den nuvarande kassan inte räcka för att nå break even, varför Bolaget förväntas behöva genomföra ytterligare en kapitalanskaffning under H2-2019.
Analyst Comments
Kommentar på AcuCorts Q4-rapport
2021-02-19
AcuCort publicerade igår den 18 februari 2021 sin delårsrapport för fjärde kvartalet 2020. Följande är vår uppföljning av rapporten, vad vi främst fokuserat på samt ett urval av senast händelser kring AcuCort.
- Tillgänglig likviditet och kapitalförbrukning
- Lägre kostnadsbas under Q4
- Godkännande för Covid-19-behandling
- Vad vi har att se fram emot 2021
- Nyligen genomförd VD-intervju med AcuCort
Tillgänglig likviditet och kapitalförbrukning
Med tanke på det utvecklingsarbetet som AcuCort har fokuserat på, och en kommersialiseringsfas som fortfarande är i sin linda, finns ännu ingen försäljning vilket i kombination med nödvändiga investeringar och rörelsekostnader resulterar i ett negativt kassaflöde. Det i sig är inte konstigt, samtidigt som det blir viktigt att effektivt nyttja den likviditeten som finns i bolaget. Vid utgången av fjärde kvartalet uppgick kassan till ca 24 MSEK, vilket kan jämföras med ca 26 MSEK vid utgången av september (Q3-20). Under sista kvartalet 2020 var därmed bolagets operativa kapitalförbrukning, s.k. burn rate, låg och sett till helåret 2020 har denna uppgått till i genomsnitt -0,7 MSEK/månad, vilket vi också anser är lågt och således något vi ser positivt på. Under kommande kvartal räknar vi dock med att AcuCort kommer ha en något högre kapitalförbrukning, vilket är helt naturligt med tanke på den kommande kommersialiseringen. Med det sagt, och med tanke på den utgående kassan per den sista december, anser vi fortsatt att AcuCort har en mycket stark finansiell position.
Lägre kostnadsbas under Q4
AcuCorts rörelsekostnaderna har under sista kvartalet 2020 varit lägre än förväntat, vilket bolaget skriver i huvudsak är på grund av senarelagda kompletterande utvecklingsaktiviteter. Under Q4-20 minskade de externa kostnader med 5 %, från -1,42 MSEK till -1,35 MSEK, och personalkostnaderna minskade med 21 %, från -0,74 MSEK till -0,58 MSEK. Detta har i sin tur bidragit till den ovannämnda låga kapitalförbrukningen som AcuCort uppvisar.
Godkännande för Covid-19-behandling
AcuCort meddelade den 3 februari att det svenska Läkemedelsverket har godkänt bolagets läkemedel ISICORT® för behandling av patienter med Covid-19 som behöver syrgasbehandling. Det godkännande som AcuCort har erhållit avser den svenska marknaden och vår bedömning är att ISICORT® kan komma att fylla ett viktigt behov inom vården. Covid-19-vaccin har rullats ut löpande sedan ett par veckor tillbaka, men ännu är vi långt ifrån en fullgod vaccinering av den svenska populationen. Innan vi når den punkten så finns det ett stort värde av alla typer av produkter, behandlingar, hjälpmedel och läkemedel som kan bidra till en bättre vård av patienter som insjuknat i Covid-19. För AcuCorts del så kan det svenska marknadsgodkännandet och den nu också utökade indikationen komma väl till hands i samband med kommande ansökningar om marknadsgodkännande på fler marknader inom exempelvis Europa och USA. Vi vet också sedan tidigare att AcuCort befinner sig i partnerdialoger avseende den bredare kommersialiseringen av ISICORT®, och det är rimligt att anta att det nyligen erhållna godkännandet för behandling av covid-19-patienter i Sverige stärker AcuCorts position i dessa dialoger.
Vad vi har att se fram emot 2021
Under 2021 kommer AcuCort att lägga ett stort fokus kring aktiviteter för kommersialiseringen av ISICORT®. Precis som bolaget kommunicerat tidigare så kommer detta innebära att fortsätta driva på de pågående dialogerna med tänkbara kommersiella partners som tillsammans med AcuCort kan ansvara för försäljning och marknadsföring av ISICORT® på de lokala marknaderna. AcuCort bedriver även ett intensivt arbete med allt övrigt som behöver vara på plats innan ISICORT® kan vara tillgängligt på marknaden, som t.ex. nationell pris- och subventionsansökan, kommersiell produktion och logistik. Kommunikation från AcuCort rörande framsteg inom dessa processer kan utgöra bra värdedrivare i aktien under 2021.
Nyligen genomför VD-intervju med AcuCort
I samband med pressmeddelandet från den 3 februari vi i kontakt med Jonas Jönmark, VD på AcuCort. Intervjun publicerade vi den 5 februari, och återfinns i sin helhet även här.
Vad betyder godkännandet för AcuCort och när tror du att ni kan börja nå ut med produkten till marknaden?
Det är mycket positivt att Läkemedelsverket har godkänt vårt läkemedel ISICORT® även för behandling av covid-19-patienter. Den utökade indikationen är ytterligare en extern kvalitetsstämpel på vårt arbete och en validering av ISICORT®. Vidare innebär det att sjukvården framgent kan få möjlighet att behandla patienter under syrgasbehandling med ISICORT®. Vår ambition är att ISICORT® kan bli ytterligare ett behandlingsalternativ i kampen mot covid-19.
Indikationen kommer också att finnas med i våra kommande ansökningar om marknadsgodkännande på fler marknader, där vi nu undersöker möjligheterna att få så kallad Fast Track, d.v.s. en påskyndad registreringsprocess som är möjlig för läkemedel avsedda att behandla covid-19-patienter. Vidare styrker den utökade indikationen oss i våra partnerdialoger och i processen att kommersialisera ISICORT®.
Just nu pågår fortlöpande dialoger med potentiella framtida partners som tillsammans med AcuCort kan ansvara för försäljning och marknadsföring av ISICORT® på de lokala marknaderna. Parallellt med dessa aktiviteter fortgår arbetet med allt annat som behöver vara på plats innan den första patienten kan behandlas med ISICORT®. Jag kan inte idag spekulera i när produkten kan tänkas bli tillgänglig på marknaden. Det är flera viktiga steg och processer som behöver hanteras omsorgsfullt, bland annat godkännande av AcuCorts nationella pris- och subventionsansökan, förberedelser för kommersiell produktion och logistik. Vissa av våra aktiviteter är mer tidskrävande än andra, men sammantaget kan jag bekräfta att aktiviteterna hittills fortlöper utan förseningar.
Vi kommer inom kort att återkomma med en uppdaterad aktieanalys.
Kommentar på AcuCorts godkännande för Covid-19-behandling
2021-02-05
AcuCort meddelade den 3 februari att det svenska Läkemedelsverket har godkänt bolagets läkemedel ISICORT® för behandling av patienter med covid-19 som behöver syrgasbehandling.
Studien som riktade strålkastarljuset mot kortisonet dexametason
Den 16 juni 2020 publicerade Reuters, Sveriges Radio med flera medier nyheten om att forskare i Storbritannien hade upptäckt att behandling med kortisonsubstansen dexametason, vilket är den aktiva substansen i AcuCorts produkt ISICORT®, kan reducera dödligheten bland personer som insjuknat i covid-19. I studien, som genomfördes vid Oxford University, konstaterades en minskad dödlighet om 35% för de patienter som behandlades med dexametason och andningshjälp med respirator, jämfört med de patienter som fick hjälp att andas endast med respirator. I den grupp av patienter som behandlades med syrgas, och dessutom fick behandling med dexametason, minskade dödligheten med 20%. Då kortisonsubstansen dexametason visade en ökad överlevnad i covid-19-patienter fick nyheten stor uppmärksamhet runt om i världen.
Sedan dess har AcuCort fortsatt att följa utvecklingen av möjligheterna till att behandla covid-19-patienter med dexametason. Efter att ISICORT® i oktober 2020 blev godkänt av Läkemedelsverket, har bolaget ansökt om att även få indikationen – behandling av covid-19 godkänd. Den 3 februari kom godkännandet från Läkemedelsverket avseende den utökade indikationen för AcuCorts ISICORT®.
”Det godkännande som AcuCort har erhållit avser den svenska marknaden och vår bedömning är att ISICORT® kan komma att fylla ett viktigt behov inom vården. Covid-19-vaccin har rullats ut löpande sedan ett par veckor tillbaka, men ännu är vi långt ifrån en fullgod vaccinering av den svenska populationen. Innan vi når den punkten så finns det ett stort värde av alla typer av produkter, behandlingar, hjälpmedel och läkemedel som kan bidra till en bättre vård av patienter som insjuknat i covid-19. För AcuCorts del så kan det svenska marknadsgodkännandet och den nu också utökade indikationen komma väl till hands i samband med kommande ansökningar om marknadsgodkännande på fler marknader inom exempelvis Europa och USA. Vi vet också sedan tidigare att AcuCort befinner sig i partnerdialoger avseende den bredare kommersialiseringen av ISICORT®, och det är rimligt att anta att det nyligen erhållna godkännandet för behandling av covid-19-patienter i Sverige stärker AcuCorts position i dessa dialoger”, säger ansvarig analytiker på Analyst Group.
I samband med bolagets pressmeddelande har vi varit i kontakt med Jonas Jönmark, VD på AcuCort.
Vad betyder godkännandet för AcuCort och när tror du att ni kan börja nå ut med produkten till marknaden?
Det är mycket positivt att Läkemedelsverket har godkänt vårt läkemedel ISICORT® även för behandling av covid-19-patienter. Den utökade indikationen är ytterligare en extern kvalitetsstämpel på vårt arbete och en validering av ISICORT®. Vidare innebär det att sjukvården framgent kan få möjlighet att behandla patienter under syrgasbehandling med ISICORT®. Vår ambition är att ISICORT® kan bli ytterligare ett behandlingsalternativ i kampen mot covid-19.
Indikationen kommer också att finnas med i våra kommande ansökningar om marknadsgodkännande på fler marknader, där vi nu undersöker möjligheterna att få så kallad Fast Track, d.v.s. en påskyndad registreringsprocess som är möjlig för läkemedel avsedda att behandla covid-19-patienter. Vidare styrker den utökade indikationen oss i våra partnerdialoger och i processen att kommersialisera ISICORT®.
Just nu pågår fortlöpande dialoger med potentiella framtida partners som tillsammans med AcuCort kan ansvara för försäljning och marknadsföring av ISICORT® på de lokala marknaderna. Parallellt med dessa aktiviteter fortgår arbetet med allt annat som behöver vara på plats innan den första patienten kan behandlas med ISICORT®. Jag kan inte idag spekulera i när produkten kan tänkas bli tillgänglig på marknaden. Det är flera viktiga steg och processer som behöver hanteras omsorgsfullt, bland annat godkännande av AcuCorts nationella pris- och subventionsansökan, förberedelser för kommersiell produktion och logistik. Vissa av våra aktiviteter är mer tidskrävande än andra, men sammantaget kan jag bekräfta att aktiviteterna hittills fortlöper utan förseningar.
Kommentar på AcuCorts Q3-rapport
2020-11-13
AcuCort publicerade idag den 13 november 2020 sin delårsrapport för tredje kvartalet 2020. Följande är vår uppföljning av rapporten.
Rapporten i sig innehöll inte några större överraskningar och var väl i linje med våra förväntningar. Vi upplever att AcuCort befinner sig i en verksamhetsmässigt stark trend, där organisationen har tagit flera kliv framåt under det senaste halvåret där viktiga milstolpar har uppnåtts. Om AcuCort kan exekvera sin lagda strategi för kommersialisering av ISICORT®, parallellt med marknadsgodkännande på fler marknader, anser vi att det finns en fortsatt god uppsida i aktien från dagens nivåer.
Närliggande värdedrivare och triggers:
- Uppdatering kring processerna för pris- och subventionsansökan, förberedelser för kommersiell produktion och logistik samt implementering och godkännande av ett uppdaterat kvalitetssystem som möjliggör partihandelstillstånd.
- Uppdateringar kring ansökningsprocesser om marknadsgodkännande för ISICORT® på fler marknader.
- Eventuell kommunikation gällande de dialoger som redan pågår med potentiella framtida partners som tillsammans med AcuCort kan ansvara för försäljning och marknadsföring av ISICORT®.
- En ytterligare potentiell värdedrivare som inte ska glömmas bort är att forskare tidigare i år upptäckte att kortisonsubstansen dexametason, vilken AcuCorts produkt ISICORT® är baserad på, kan reducera dödlighetsgraden bland personer smittade av Covid-19. Exakt vilken väg detta kan ta för AcuCort och vilken möjlighet som finns att söka indikation för Covid-19 för ISICORT®, är för tidigt att säga, men likväl en intressant punkt i den långsiktiga investeringsidén.
En viktig parameter som nämns i rapporten är att ISICORT® har uppnått två års stabilitetsdata, vilket innebär att ISICORT® klarar av minst två års lagerhållbarhet. Detta är en minst sagt stor fördel, och av yttersta vikt, inför den kommande kommersialiseringen.
Världen har under året blivit en annorlunda plats, men AcuCort går till synes från klarhet till klarhet och checkar enligt Analyst Group av delmål efter delmål. Vägen mot kommersialisering känns väl utstakad där AcuCort verkar ha en klar och tydlig uppfattning om vad de måste göra för att lyckas fortsätta leverera värde till aktieägarna. Vi ser fortsatt positivt på AcuCort som investeringsidé och kommer inom kort att återkomma med en uppdaterad aktieanalys.
Intervju med AcuCorts VD Jonas Jönmark i samband med marknadsgodännande av ISICORT
2020-10-12
Den 7 oktober 2020 kommunicerade AcuCort att bolaget erhållit marknadsgodkännande av det svenska Läkemedelsverket för läkemedlet ISICORT®. Analyst Group har i samband med detta kontaktat VD Jonas Jönmark på AcuCort som nu återkommit med en kort intervju.
Skulle du kunna börja med att sammanfatta vad det egentligen innebär för er att ISICORT® nu erhållit ett marknadsgodkännande?
Marknadsgodkännandet är en viktig milstolpe för AcuCort och bolagets första innovativa läkemedel ISICORT®. Godkännandet betyder mycket mer än att läkemedlet är godkänt för kommersialisering och behandling av patienter på den svenska marknaden. Det är även en kvalitetsstämpel från Läkemedelsverket att ISICORT® håller vad vi lovar, både vad gäller effekt och säkerhet samt att vi som bolag lever upp till de högt ställda kvalitetskraven som ställs på oss. Det är ett hårt arbete och en lång process innan ett läkemedel får ett godkännande och det är långt ifrån alla kandidater som når så långt. Att vi rundat milstolpen är både glädjande och inspirerande, och stärker vår bedömning att tiden fram till kommersialisering kan vara relativt kort. Nu kan vi fortsätta att lägga full kraft på implementeringen av vår affärsstrategi.
Kan du utveckla lite mer gällande hur ert nästa steg i er affärsstrategi kommer att se ut, vilka insatser ni kommer fokusera på närmast och vad som måste komma på plats fram tills att den faktiska försäljningen kan påbörjas?
Sverige och det svenska Läkemedelsverket har inom life science-sektorn ett mycket högt anseende i världen. Att vi har erhållit ett marknadsgodkännande i Sverige som första land är en styrka när vi nu kommer att söka godkännanden på fler marknader. ISICORT® är på god väg mot kommersialisering. Arbete som pågår nu är förberedelser för ansökan om marknadsgodkännande på fler marknader, dialoger med potentiella partners för kommersialisering samt ansökan om pris och subventionering, vilket också det sker per land. De partners vi för dialoger med är de som i kommersialiseringen kommer att, tillsammans med AcuCort, ansvara för försäljningen och marknadsföringen av ISICORT® i sina länder och regioner.
Om du för en investerare skulle belysa något som du tycker är extra viktigt att bevaka/hålla utkik efter i närtid, vad skulle du vilja lyfta fram då?
Mycket pågår parallellt och vissa processer kommer naturligtvis att ta längre tid än andra, men med ett marknadsgodkännande i Sverige står vi väl rustade i vår tillväxtresa. Tre viktiga milstolpar framöver skulle jag säga är ytterligare marknadsgodkännanden, godkänt pris och subventionering samt avtal med partners för kommersialisering.
Kommentar på AcuCorts Q2-rapport
2020-08-28
AcuCort publicerade idag den 28 augusti 2020 sin delårsrapport för andra kvartalet 2020. Följande är vår uppföljning av rapporten.
Under årets andra kvartal har AcuCort arbetat intensivt med att ta fram bra underlag till Läkemedelsverket för bolagets ansökan om ett nationellt marknadsgodkännande av ISICORT®. Precis som vi nämnt i vår senaste aktieanalys av AcuCort så tror vi att ISICORT skulle kunna närma sig marknadsgodkännande i Sverige mot slutet av 2020, och att försäljningen då skulle kunna påbörjas under 2021. Ett initialt marknadsgodkännande anses utgöra en potentiellt stark värdedrivare i aktien. ISICORT har som känt väsentliga patientfördelar vilket dessutom ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt och således ytterligare värdeutveckling i aktien.
Parallellt med arbetet för nationellt marknadsgodkännande har AcuCort under Q2-20 även drivit på bolagets övriga utvecklingsarbete, med bl.a. ett flertal partnerdialoger. Vad dessa dialoger kan resultera i är svårt att säga idag, men med tanke på ISICORT:s fördelar och det läget som AcuCort befinner sig i, är det inte omöjligt att positiva överraskningar skulle kunna dyka upp framöver.
En extra krydda finns även i form av de delresultat som Oxforduniversitetet rapporterade från en studie som bl.a. visade att behandling med dexametason, den aktiva beståndsdelen i ISICORT, eventuellt kan ha en positiv effekt på patienter med svåra symptom från Covid-19. Baserat på de preliminära resultaten har den europeiska läkemedelsmyndigheten startat en undersökning om möjligheterna att behandla Covid-19-patienter med dexametason. Det vore såklart minst sagt intressant om AcuCort skulle kunna bidra till att minska dödligheten i rådande pandemi, men som alltid blir det massor av frågor på vägen; vilka doseringar är aktuella, ska intensivvårdspatienter kanske bara injiceras, vad kostar munfilm jämfört med befintliga tabletter osv. Det är således alldeles för tidigt för att göra några konkreta beräkningar kring vad den tänkbara potentialen för AcuCort kan vara, men likväl en intressant faktor att fortsatt bevaka.
Med tanke på det utvecklingsarbetet som AcuCort just nu fokuserar på, finns ännu ingen försäljning vilket i kombination med nödvändiga investeringar och rörelsekostnader resulterar i ett negativt kassaflöde. Det i sig är inte konstigt, samtidigt som det blir viktigt att bevara den likviditeten som finns i bolaget. Vid utgången av kvartalet uppgick kassan till ca 28 MSEK, vilket kan jämföras med ca 31 MSEK vid utgången av mars i år. Under H1-20 uppgick bolagets operativa kapitalförbrukning, s.k. burn rate, till ca -0,8 MSEK/månad, vilket vi anser är lågt och således något vi ser positivt på. En viktig faktor att ta i beaktande är hur länge nuvarande likviditet räcker till. Med avstamp i den utgående kassan per juni månad, historisk burn rate och en uppskattning kring framtida kapitalbehov, räknar vi med att AcuCort är finansierade en bra bit in i 2021.
I samband med rapporten har vi även varit i kontakt med Jonas Jönmark, VD på AcuCort.
Tidigare i augusti tillträdde du som VD för AcuCort. Kan du berätta lite mer om vad det var med AcuCort som fångade ditt intresse?
”AcuCort har funnits på min radar en längre tid, varför jag är extra glad över att få vara en del i att ta bolaget till nya nivåer. AcuCort är ett företag, som med sin innovativa produkt, kan göra stora skillnader för patienter världen över och som jag ser det så står vi väl rustade för att ta vår produkt till marknaden.”
Vi kommer inom kort att återkomma med en uppdaterad version av vår senaste aktieanalys.
Kommentar gällande AcuCorts framsteg i ansökningsprocess
2020-07-20
Den 15 juli 2020 meddelade AcuCort att de bekräftar framsteg i ansökningsprocessen om nationellt marknadsgodkännande för ISICORT®.
“Senaste månaden har AcuCort-aktien rört sig sidledes, samtidigt som bolaget fortsätter att ta steg i rätt riktning. Vi behåller därmed vår värderingsansats där vi fortsatt ser ett riskjusterat nuvärde om ca 6 kr per aktie i ett Base scenario”, säger ansvarig analytiker på Analyst Group.
Kort sammanfattning av nyheten
- AcuCort har mottagit den andra utvärderingsrapporten (Second Round Assessment Report) från Läkemedelsverket i juli enligt plan.
- Efter AcuCorts utvärdering av de återstående frågorna, och med stöd av bolagets regulatoriska expertispartner samt styrelsens ytterligare granskning, är slutsatsen att en stor del av frågorna har besvarats väl och att de utestående frågorna är hanterbara.
- AcuCort kommer att lämna in svarsdossiern avseende den andra utvärderingsrapporten den 11 augusti 2020.
Ansvarig analytiker kommenterar
“Med hänsyn till formuleringarna om att frågorna har besvarats väl, att de utestående frågorna är hanterbara och att AcuCort känner sig säkra på planeringen framöver, ser vi att det är fortsatt sannolikt att ISICORT skulle kunna närma sig marknadsgodkännande i Sverige mot slutet av 2020 och att försäljningen då estimeras kunna påbörjas under 2021. Senaste månaden har AcuCort-aktien rört sig sidledes, samtidigt som bolaget fortsätter att ta steg i rätt riktning. Vi behåller därmed vår värderingsansats där vi fortsatt ser ett riskjusterat nuvärde om ca 6 kr per aktie i ett Base scenario”, säger ansvarig analytiker på Analyst Group.
Ny VD rekryterad
Den 16 juli kom nyheten att rekryteringen av en permanent VD har avslutats och att Jonas Jönmark tillträder som VD den 9 augusti 2020. Jonas har en MBA-examen från Lunds universitet och över 20 års erfarenhet från ledande befattningar och VD-positioner inom läkemedelsindustrin och life science-sektorn. Hans karriär har inkluderat stora internationella läkemedelsföretag som bland annat Pfizer AB, Astellas Pharma A/S och Astra Zeneca Sweden, men också mindre startupbolag som Life Science Support AB och Alteco Medical AB. Jonas har en bred erfarenhet av internationella produktlanseringar, etablering av sälj- och distributionskanaler, kommersiella partnerskap, prissättnings- och ersättningsförhandlingar med myndigheter samt internationell affärsutveckling inom life science.
I samband med att Jonas tillträder som VD under augusti ämnar vi återkomma med en VD-intervju.
Intervju med AcuCorts VD Ann Gidner
2020-06-18
Den 16 juni 2020 publicerades information av Reuters, Sveriges Radio med flera att forskare i Storbritannien har upptäckt att kortisonsubstansen dexametason, vilken AcuCorts produkt ISICORT® är baserad på, kan reducera dödsgraden bland personer smittade av Covid-19. AcuCorts aktie steg kraftigt på nyheten och senaste dygnet har vi uppmärksammat flera dialoger på diverse aktieforum online. Analyst Group har i samband med detta kontaktat VD Ann Gidner på AcuCort för en kort intervju.
Skulle du kunna börja med att helt enkelt sammanfatta vad det egentligen är för något som forskare har upptäckt gällande dexametason och dess effekt på Covid-19?
Det är en opublicerad studie från Oxford University i Storbritannien, där man såg 35 % minskad dödlighet för de patienter som enbart kunde andas med hjälp av respirator och som fick dexametason. Bland de som behandlades med syrgas, minskade dödligheten med 20 %. I förlängningen bidrog läkemedlet till att en av åtta patienter med respirator överlevde. För patienter som fick syrgas överlevde en av 25.
Eftersom dexametason är det första läkemedlet som har visat sig öka överlevnaden i Covid-19, är det här en nyhet som fått stor uppmärksamhet runt om i världen.
Vad får denna upptäckt för effekt på er nuvarande utvecklingsstrategi och fokusområde?
Vår nuvarande utvecklingsstrategi förändras inte i dagsläget, vi driver processen för godkännande av ISICORT vidare, och dessa nyheter påverkar inte den befintliga ansökningsprocessen hos Läkemedelsverket. När man väl gått in med ansökan så är det den man får svar på. Likadant så har vi samma fortsatta plan för fler europeiska länder och för en ansökan i USA, där löper arbetet på. Sen kan en omfattande positiv publicitet kring substansen dexametason ändå vara lite hjälp på vägen för ISICORT indirekt, om myndigheter med flera har tagit del av de positiva nyheterna – då det blir mer kännedom om hur dexametason hjälper patienter generellt.
Ser du det som tänkbart att AcuCort skulle kunna etablera ett segment som riktar sig mot behandling av personer smittade av Covid-19?
När denna och andra pågående studier publiceras, så kan man granska resultaten. Det pågår flera studier med olika förutsättningar, olika doseringar m.m. Om den positiva effekten bekräftas – och det kan bedömas finnas ett fortsatt behov – så kommer AcuCort att kunna ta ställning till ett nytt segment för behandling av den här typen av patienter. Det vore ju fantastiskt att kunna bidra till att minska dödligheten i en svår pandemi. Sen blir det massor av frågor på vägen – vilka doseringar är aktuella, ska intensivvårds-patienter kanske bara injiceras, vad kostar munfilm jämfört med befintliga tabletter, osv – så det är alldeles för tidigt att ge några besked om en tänkbar potential i någon form.
Hur Analyst Group ser på AcuCort som investering
AcuCorts produkt ISICORT® skulle kunna närma sig marknadsgodkännande i Sverige mot slutet av 2020 och försäljningen estimeras då påbörjas under 2021. ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till 3,4 mdUSD, och ledning och styrelse anses inneha rätt kompetenser för att utveckla Bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat potentiellt nuvärde om ca 115 MSEK, motsvarande 6 kr per aktie, i ett Base scenario.
Analyst Groups kommentar kring patentansökans uppdatering
2020-05-29
AcuCort publicerade igår den 28 maj 2020 en kommentar kring uppdatering avseende bolagets andra patentansökan i USA.
”Vi kan förstå att marknadens initiala reaktion är negativ, men vid en djupare analys anser vi att den negativa kursrörelsen är en överreaktion”, säger ansvarig analytiker på Analyst Group.
Tidigare i veckan gjorde det amerikanska patentverket (the US Patent and Trademark Office, USPTO) en uppdatering på sin hemsida avseende AcuCorts andra patentansökan för ISICORT®. Ansökan har fått statusen”Final Rejection Counted, Not Yet Mailed”. Vad det här betyder är att ansökan i dess nuvarande form inte är godkänd samt att AcuCort ännu inte har informerats.
Med en rubriksättning som innehåller ”Final Rejection” kan vi förstå att marknaden reagerar negativt och att aktien som en konsekvens handlades ned under onsdagen den 27 maj. Samtidigt är det på sin plats att ett förtydligande görs kring vad detta faktiskt innebär, där ansökans status, vilken vid en första anblick kan kännas nedslående, inte alls behöver vara så negativ som den kan verka vara. Det är nämligen normalt, och nästan praxis, att handläggare på USPTO utfärdar en eller flera s.k. Office Actions. En handläggare har nämligen endast begränsad tid att pröva en patentansökan och fatta beslut om ansökan ska beviljas eller avslås. För att påskynda en sådan slutsats utfärdar handläggarna ofta en s.k. Final Office Action, eller då Final Rejection. Detta är dock inte ett slutligt beslut att avslå ansökan. Tvärtom, den sökande, i detta fall AcuCort, har ett antal möjligheter att fortsätta granskningen av ansökan, bland vilka kan nämnas: 1) lämna in en begäran om fortsatt granskning, 2) lämna in en ändring i ansökan, 3) lämna in en fortsatt eller uppdelad ansökan, eller 4) lämna in ett överklagande.
Patterson Thuente, en amerikansk advokatbyrå som specialiserar sig på immateriella rättigheter (bl.a. patentansökningar), skriver att under processen för en amerikansk patentansökan kan en andra eller efterföljande Office Actions göras ”Finala” av granskaren. ”Final” är dock en felaktig anmärkning eftersom ett slutligt avslag inte betyder att ansökan för patentet har misslyckats. Det finns faktiskt flera tillgängliga alternativ för att gå vidare med ansökan, exempelvis någon av de fyra alternativ som nämns ovan.
För mer information om hur Patterson Thuente beskriver hur en patentansökan kan gå till i USA och vilka alternativ som finns, läs gärna originalartikeln via följande länk.
”Det är klart att en status om att ansökan godkänts eller gått vidare hade varit mer positiv, men samtidigt är inte USPTO:s utlåtande så negativt som det kan verka. Precis som AcuCort skriver så genomgår patentansökningar i USA ofta flera steg, där man kan fortsätta med fler argument för att få igenom sin ansökan. Vi kan förstå att marknadens initiala reaktion är negativ, men anser samtidigt att kursrörelsen är en överreaktion. Vi ser fortsatt god uppsida i AcuCort och ser ingen anledning att förändra vårt värderingsintervall där vi ser ett motiverat värde om 6,0 kr per aktie i ett Base scenario”, säger ansvarig analytiker på Analyst Group.
I samband med AcuCorts kommentar av uppdateringen avseende den andra patentansökan i USA, har vi varit i kontakt med VD Ann Gidner för hennes kommentar och syn på statusuppdateringen från USPTO.
”AcuCort har redan skydd för ISICORT i USA, genom patentet ”Acute Glucocorticoid Therapy”. Detta patent beskriver medicinsk självbehandling med glukokortikoider i akuta situationer och är giltigt fram till slutet av 2028. För att ytterligare skydda produkten och förlänga exklusiviteten har vi sedan ansökt om ett andra patent vad gäller formuleringen, tillverkningsprocessen och tänkt användningsområde. Det är ett vanligt tillvägagångssätt, att bygga IP-skydd i flera lager runt sin produkt. Även om vi inte lyckades få det andra patentet godkänt i USA i första försöket, så är det bara att arbeta vidare. Vi har duktiga patentjurister som tar sig an detta.”, säger Ann Gidner, t.f. VD på AcuCort.
Kommentar på AcuCorts delårsrapport
2020-04-29
AcuCort publicerade igår den 28 april 2020 sin delårsrapport för första kvartalet 2020. Följande är vår uppföljning på rapporten.
Under februari erhöll AcuCort den första utvärderingsrapporten från Läkemedelsverket av den nationella ansökan om marknadsgodkännande för ISICORT®. Sedan dess har AcuCort lagt ett stort fokus på att ta fram goda underlag för att beskriva produktionsprocessen i mer detalj. Arbetet med svarslistan har även krävt avvägningar i regulatoriska och dokumentationsrelaterade frågor.
Vi har i samband med Q1-rapporten varit i kontakt Ann Gidner, interim VD på AcuCort, för att be henne sammanfatta hur de senaste veckorna fortlöpt för AcuCort.
”Utbrottet av Covid-19 har fått stor påverkan på världen i stort. För AcuCort bedömer vi dock för närvarande att påverkan är begränsad. I nuläget är samarbetet med vår tillverkningspartner och våra regulatoriska experter av stor vikt, och dessa har säkrat en fortlöpande verksamhet med bibehållen kvalitetsnivå. Vi själva har under en tid arbetat en hel del på distans och jag skulle vilja säga att det fungerar bra för oss och ger god koncentration i det nuvarande arbetet med dokumentation. Senaste veckorna har vi som nämnt arbetat intensivt med svarslistan för Läkemedelsverket. I och med att vi nu lägger mindre tid på exempelvis resor till följd av Covid-19, har vi kunnat lägga bra fokus på arbetet med den här rapporten. Vi har också arbetat vidare med en rad praktiska områden, som produktionsplanering, produktutveckling och prissättning”, säger Ann Gidner.
AcuCort ska lämna in sin rapport till Läkemedelsverket den 8 maj.
Under mars deltog AcuCort på BIO-Europe Spring, följande är Ann Gidners sammanfattning av hur konferensen gick:
”Den stora läkemedels- och partnering-konferensen BIO-Europe Spring som skulle hållas fysiskt i Paris under mars blev istället ett digitalt event. Det digitala upplägget funkade förvånansvärt bra och de möten vi hade kändes effektiva och givande. Under konferensveckan hade vi många intressanta möten och dialoger med gott resultat, jag hoppas att vi framöver kan kommunicera mer om detta till marknaden.”
Vi kommer inom kort att återkomma med en uppdaterad aktieanalys.
Analyst Group följer upp AcuCorts kommuniké med en kommentar och VD-intervju
2020-02-26
AcuCort publicerade igår den 25 februari 2020 sin bokslutskommuniké för 2019. Vi har i samband med rapporten kontaktat VD Ann Gidner för att ställa några korta frågor.
Nu är det ungefär två månader sedan du tillträdde som interim VD för AcuCort. Kan du berätta lite mer om vad det var med AcuCort som fångade ditt intresse?
Ja det har varit en intensiv och rolig period att starta upp. AcuCort är ett bolag i spännande läge, eftersom man har en produkt så nära marknad som kan göra riktigt bra patientnytta. För mig personligen är AcuCort väldigt intressant eftersom det inte handlar om ett rent forskningsbolag med många år kvar till marknaden utan en mer mogen fas av kommersialisering och affärsbygge, vilket är min specialitet. Mer precist är det i nuläget mycket viktigt med partnerskap för AcuCort, och jag har bland annat en mångårig bakgrund som internationell Licensierings-direktör för just drug delivery-teknologi.
Under januari 2020 meddelade ni en positiv syn på att utfallet i den andra bioekvivalensstudien för USA inte är ett hinder för att ansöka om marknadsgodkännande av ISICORT® på USA-marknaden. Kan du berätta lite mer om hur du ser på ert kommande arbete kring USA-registreringen?
Det stämmer, tack vare samarbete med vår expertgrupp kom vi fram till en bra plan. Nu ska vi utforma hur den primära planeringen kan tillämpas med den ansökningsväg som är aktuell, och vi tar in lärdomar från processen i Sverige.
Tidigare i februari meddelade ni att ni mottagit den första utvärderingsrapporten från Läkemedelsverket som svar på den nationella ansökan om marknadsgodkännande för ISICORT® i september 2019. Kan du berätta lite mer om hur ni ser på utvärderingen och vad nästa steg blir härifrån?
Ja, Läkemedelsverket har gjort ett gediget arbete. Vi ser ganska många frågor på tillverkningen av munfilmen, vilket troligen hänger ihop med att det just är en nyare administrationsform, inte som vanliga tabletter. Sen i klinik-delen känns det som ett gott mottagande, vilket blir roligt att beskriva mer när vi kommit längre i dialogen med myndigheten. Rapporten har inga formella starka invändningar, vilket är glädjande.
Nu jobbar vi på med att sammanställa kompletterande data och beskrivningar tillsammans med framför allt vår skickliga tillverkningspartner i Frankrike. I maj månad ska vi lämna in svaren, och sedan följer en ny utvärderingsperiod, så vi vet mer framåt halvårsskiftet.
Vad kommer vara ditt och AcuCorts främsta fokus under 2020?
Ett huvudfokus är givetvis det fortsatta arbetet för att nå en färdig produktregistrering för ISICORT i Sverige. Det är en mycket stor milstolpe, och den ger oss lärdomar för det arbetet med Europa och USA. Jag vill också bygga bolagets position och nätverk i en rad olika sammanhang och med dialoger kring licensiering i synnerhet.
Ansvarig analytiker på Analyst Groups kommenterar sin syn på AcuCort som investering
”ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. Bolagets adresserbara marknad bedöms uppgå till omkring 3,4 miljarder dollar, och nuvarande ledning och styrelse anses inneha rätt kompetenser för att utveckla bolaget i en positiv riktning. Genom en rNPV-värdering ges ett riskjusterat nuvärde om 5,2 kronor per aktie i ett Base scenario och 9,3 kronor i ett Bull scenario. Vi ser således en fortsatt uppsida i aktien från dagens nivåer”, säger ansvarig analytiker.
Kommentar inför AcuCorts bokslutskommuniké
2020-02-24
AcuCort publicerar imorgon den 25 februari 2020 sin bokslutskommuniké för 2019. Följande är våra tankar inför rapporten.
”AcuCort har inlett året med starkt positiva nyheter, i samband med rapporten hoppas vi få läsa mer om dessa,” säger ansvarig analytiker på Analyst Group.
För ungefär en månad sedan meddelade AcuCort en positiv syn på att utfallet i den andra bioekvivalensstudien för USA inte är ett hinder för att ansöka om marknadsgodkännande av bolagets läkemedelskandidat ISICORT® på USA-marknaden. Som vi nämnt i vår tidigare kommentar av pressmeddelandet var nyheten minst sagt välkommen där den tillsatta expertgruppen bland annat presenterade handlingsalternativ för att möjliggöra registrering och kommersialisering av ISICORT på den amerikanska marknaden. Det känns även extra betryggande att dessa slutsatser bekräftades av ytterligare två oberoende expertinstanser i USA och Tyskland. Även om kanske ingen ny information kommer att framgå, hoppas vi likväl i samband med morgondagens rapport att få läsa mer om Ann Gidners egna tankar i sitt VD-ord om hur bolaget ser på arbetet kring USA-registreringen.
Under september 2019 lämnade AcuCort in en nationell hybridansökan för marknadsgodkännande av ISICORT till svenska Läkemedelsverket. För mindre än två veckor sedan meddelade AcuCort att myndigheten återkommit med den första utvärderingsrapporten inklusive en översikt och en frågelista. I kommunikationen framgår det att ”[…] Det gavs inga formella starka invändningar (s.k. major objections), och den initiala analysen av rapporten och frågelistan tyder inte på några stora stötestenar.” Att inga starka invändningar eller stora stötestenar fanns är såklart något vi anser är minst sagt positivt. Baserat på aktiens relativt neutrala reaktion på dagen för pressmeddelandet, tror vi att marknaden har missat detta. I morgondagens VD-ord hoppas vi att mer information kan ges kring nyheten, vilket i sig skulle kunna bidra till att marknaden inser nyhetens fulla värde.
I samband med bokslutskommunikén kommer vi att återkomma med en kort kommentar.
AcuCort rapporterar expertgruppens arbete med positivt utfall
2020-01-21
AcuCort meddelade igår en positiv syn på att utfallet i den andra bioekvivalensstudien för USA inte är ett hinder för att ansöka om marknadsgodkännande av bolagets läkemedelskandidat ISICORT® på USA-marknaden. Aktien reagerade minst sagt starkt och var som mest upp hela 34 %.
”Nyheten var minst sagt välkommen där expertgruppen bland annat presenterade handlingsalternativ för att möjliggöra registrering och kommersialisering av ISICORT på den amerikanska marknaden. Det känns även extra betryggande att dessa slutsatser har bekräftats av ytterligare två oberoende expertinsatser i USA och Tyskland. Aktien tog ett glädjehopp på nyheten och steg som högst till 3,45 kr i gårdagens handel, motsvarande en ökning om ca 34 procent. Vi ser fortsatt positivt på AcuCort där ISICORT har väsentliga patientfördelar vilket ger goda förutsättningar, vid läkemedelsgodkännande, för en omfattande framtida tillväxt. AcuCorts adresserbara marknad bedöms uppgå till 3,4 miljarder dollar, och nuvarande ledning och styrelse anses inneha rätt kompetenser för att utveckla AcuCort i en positiv riktning. Analyst Groups senaste rNPV-värdering visar på ett riskjusterat nuvärde om 102 MSEK, motsvarande 5,2 SEK per aktie, i ett Base scenario”, säger ansvarig analytiker på Analyst Group.
Bakgrund till vad som tidigare hänt
AcuCort meddelade i början av november 2019 att de tillsatt en expertgrupp för att utvärdera resultaten av den andra studien för USA-marknaden, med icke-fastande deltagare, där bioekvivalens uppnåddes på två parametrar av tre. Gruppen har analyserat tänkbara orsaker till avvikelsen, och har kunnat belägga den mest troliga. Denna är förknippad med att man i kliniken jämfört två olika orala farmaceutiska beredningsformer, vilket ger vissa skillnader i farmakokinetik.
I gårdagens pressmeddelande framgår information om att expertgruppen har identifierat att studiedesignen hade kunnat innehålla fler mätpunkter. AcuCorts ledning har därför tagit beslut att en farmakokinetisk modellering och simulering ska utföras av externa experter, för att säkerställa bästa möjliga kunskap om produktens uppförande i icke-fastande tillstånd vid fler mätpunkter, inför fortsatt registreringsarbete.
Kommentar från interim-VD
”Eftersom detta i USA är en 505(b)(2)-ansökan och inte en generika-ansökan, ska vissa avvikelser kunna hanteras. Då vi nu har fått de regulatoriska experternas samsyn, så har vi i AcuCort dragit slutsatsen att det finns goda möjligheter att arbeta för USA-registrering. Jag är mycket glad att kommunicera detta. Vi ser med tillförsikt fram emot fortsatt arbete med såväl Sverige- som USA-registreringen enligt plan”, säger AcuCorts interims-VD Ann Gidner.
AcuCort anställer Ann Gidner som interim VD
2019-12-13
AcuCort meddelade igår att VD Mats Lindfors avser minska sitt engagemang i bolaget på grund av familjeskäl., och att Ann Gidner är tillsatt som interim VD från den 1 januari 2020.
Ann Gidner har god erfarenhet från ledande roller inom läkemedel och life science, vilket bland annat innefattar affärsområdeschef på Inceptua GmbH, licensieringsdirektör på Albumedix A/S (Novozymes Biopharma) och VD för läkemedelsstrategibolaget Monocl AB. Gidner sitter även i styrelsen för SenzaGen AB sedan 2014. Ann Gidner är utbildad civilingenjör i bioteknik på Lunds Tekniska Högskola och har en MBA från Lunds universitet.
Nuvarande VD Lindfors kommer övergå från rollen som VD till att stödja AcuCort som konsult, där han fortsatt har ansvar för vissa projekt i AcuCorts affärsplan.
Analyst Group ser det som positivt att avgående VD behåller ett engagemang i bolaget för att underlätta övergången och för att fortsätta de pågående projekten. Vidare är det intressant att följa det arbete och eventuella förändringar som görs av den tillförordnade VDn Ann Gidner och den person som senare rekryteras som ordinarie VD.
Följande kommentarer från involverade nyckelpersoner publicerades i samband med nyheten.
– Jag är oerhört glad över att AcuCort har lyckats knyta till sig Ann Gidner som har gedigen kompetens och internationell erfarenhet inom viktiga områden för bolaget. Att vi dessutom har hittat en lösning som innebär att AcuCorts nuvarande VD Mats Lindfors kan fortsätta att arbeta aktivt som konsult tryggar kontinuitet liksom bra överlämning och ger ett resurstillskott, säger Ebba Fåhraeus, styrelseordförande i AcuCort AB.
– AcuCort är ett spännande bolag och ISICORT® är en innovativ produktkandidat med stor potential. Jag har arbetat med olika aspekter av läkemedelsutveckling och kommersialisering i hela mitt yrkesliv och ser fram emot att leda arbetet vidare mot godkännande och kommersialisering av i första hand ISICORT®, säger AcuCorts tillträdande interim-VD Ann Gidner.
– Dagens tillkännagivande upplever jag som positivt för såväl AcuCort som för mig personligen. Jag har sedan en tid önskat att förändra min arbetssituation. Min nya roll som konsult innebär att jag kan fortsätta arbeta för AcuCort, men i mer begränsad utsträckning, samtidigt som AcuCort tillförs ny kompetens och nya perspektiv. Sammantaget tycker jag att detta är en utmärkt lösning, säger AcuCorts nuvarande VD Mats Lindfors.
Uppföljning på AcuCorts Q3-19
2019-11-20
AcuCort presenterade igår den 19 november sin delårsrapport för tredje kvartalet 2019.
I rapporten noteras inga väsentliga överraskningar. Kostnadsökningen i jämförelse med det andra kvartalet och motsvarande period förra året bedöms bero på utgifter relaterade till processen för godkännande gällande ISICORT® i EU och USA.
Väsentliga händelser under kvartalet är sedan tidigare kända och innefattar främst; namnbyte till ISICORT® från Dexa ODF, ansökan för marknadsgodkännande till Läkemedelsverket, förstärkt patentskydd och genomförd nyemission om cirka 41,2 MSEK.
Efter det tredje kvartalets utgång kom nyheten att ISICORT® inte uppnådde bioekvivalens i den andra bioekvivalensstudien inför registrering i USA. Bolaget har tillsatt en expertgrupp som vidare kommer utreda orsaker till detta och potentiella vägar framåt för kommersialisering i USA. Bolaget kommer att kommunicera status i detta arbete i takt med att det fortlöper. Bioekvivalens uppnåddes på två av tre markörer, vilket innebär att förändringar behöver göras för att även uppnå rätt värde på den tredje markören.
I VD-ordet från Mats Lindfors framgår det att Bolaget gjorde fortsatta framsteg under det tredje kvartalet. Inte minst innebär nyemissionen i september att AcuCort har en starkare finansiell ställning inför det fortsatta arbetet mot kommersialisering av ISICORT® och innebär att ett eventuellt kapitalbehov inte förväntas uppstå förens en god bit in i år 2021 som tidigast. Vidare har AcuCort fått ett patent godkänt av den europeiska patentmyndigheten som förlänger patentskyddet och som enligt Lindfors kommer underlätta kommersialiseringen av ISICORT®. Patentet är samägt med den tidigare tillverkningspartnern LTS Lohmann. I VD-ordet, eller rapporten i övrigt, nämndes inget om samtal med potentiella partners för distribution eller licensiering.
Rörelseresultatet för det tredje kvartalet blev –2,61 MSEK, vilket var lägre än väntat som följd av högre övriga externa kostnader. Detta kan jämföras med –2,23 MSEK under det andra kvartalet. En trolig förklaring till dessa högre kostnader är den fortsatta processen att nå kommersialisering som innefattar regulatoriska kostnader och kostnader för genomförd bioekvivalensstudie m.m.

Vi kommer inom kort att återkomma med en uppdaterad aktieanalys.
Kommentar inför AcuCorts Q3-19
2019-11-18
Imorgon den 19 november publicerar AcuCort sin delårsrapport för tredje kvartalet 2019, följande är våra tankar inför rapporten.
Sammanfattning av händelser under hösten
Under det tredje kvartalet har de främsta händelserna varit att AcuCort skickat in ansökan om marknadsgodkännande för läkemedelskandidaten ISICORT i Sverige och nyemissionen om cirka 41,2 MSEK. Efter kvartalets utgång visade det sig att ISICORT inte uppnådde bioekvivalens i den andra bioekvivalensstudien inför registrering av läkemedelskandidaten i USA.
I slutet av september ansökte AcuCort om marknadsgodkännande för ISICORT i Sverige, som en del i planen att lansera produkten i EU. Vid ett marknadsgodkännande i Sverige kan AcuCort sedan gå vidare till ett eventuellt godkännande i fler EU-länder genom en så kallad Mutual Recognition Process. Sannolikt återkommer Läkemedelsverket med frågor till AcuCort inom några månader och det är först då det kommer visa sig om bioekvivalensstudien för registreringen i USA kommer ha några konsekvenser för ansökningsprocessen i Sverige och vidare EU. Bolaget har kommunicerat att det inte finns någon prognos om datum för eventuellt godkännande.
I slutet av augusti presenterade AcuCort en företrädesemission om 41,2 MSEK före emissionskostnader, vilket var en betydligt större emission än Analyst Group förväntat. Bakgrunden till emissionen var att Bolaget behövde kapital för den fortsatta kommersialiseringsprocessen för ISICORT.
I oktober blev resultaten från den andra bioekvivalensstudien för registrering i USA kända. ISICORT uppnådde inte bioekvivalens då värdet för en av tre markörer föll utanför det godkända intervallet. Konsekvenserna av detta är fortfarande osäkra och AcuCort att tillsatt en expertgrupp som utreder orsaker och alternativ för det fortsatta arbetet mot registrering i USA.
Fokus framgent på läkemedelsgodkännande, partnersamtal och bioekvivalens
De faktorer som investerare bör fokusera på i kvartalsrapporten och tillhörande VD-ord är enligt Analyst Groups bedömning följande:
- Läkemedelsgodkännande. AcuCort har skickat in ansökan för läkemedelsgodkännande för ISICORT i Sverige, som en del i processen att nå godkännande i fler EU-länder. Eventuella uppdateringar gällande denna process och potentiella följder av att ISICORT inte uppnådde bioekvivalens i studier för registrering i USA är viktiga att beakta för investerare.
- För att nå kommersialisering av ISICORT väntas Bolaget behöva ingå samarbete med partners för distribution och/eller licensiering. Inga konkreta samarbetspartners är kända, men enligt tidigare VD-ord förs diskussioner med flera aktörer.
- Bioekvivalens för USA-registrering. Det fortsatta arbetet med att identifiera orsaker och potentiella lösningar för att så snabbt som möjligt göra förändringar som kan leda till att bioekvivalens uppnås. Även eventuella uppdateringar gällande tidsplan och kostnader i samband med arbete mot registrering i USA är viktiga att följa.
Vi kommer att återkomma med en uppdaterad aktieanalys efter rapporten.
AcuCort uppdaterar kring bioekvivalensstudie
2019-11-11
AcuCort gav den 8 november 2019 ytterligare information om resultaten från den andra bioekvivalensstudien inför en USA registrering.
I oktober rapporterade AcuCort resultatet från den sista av två bioekvivalensstudier och läkemedelskandidaten ISICORT® uppnådde inte bioekvivalens på icke-fastande deltagare. Nu lämnar bolaget en uppdatering om det fortsatta arbetet kring bioekvivalensstudien inför USA-registrering.
Kraven för att uppnå bioekvivalens innefattar tre mätparametrar där utfallet måste vara inom ett visst intervall, som sätts i relation till en sedan tidigare godkänd referensprodukt. ISICORT® uppnådde bioekvivalens på två av tre mätparametrar, men inte på den tredje parametern (kallad Cmax) gällande den maximala mängd aktiv substans som uppmäts i plasma på deltagarna. Anledningen till att ISICORT® inte uppfyllde kravet för Cmax var att värdet var för lågt i relation till referensprodukten. ISICORT® uppfyllde inte heller kraven för parametern Tmax, vilket inte är ett krav för bioekvivalens men ändå anses viktig. Tmax beskriver hur lång tid det tar att uppnå den maximala mängden aktiv substans i plasma och AcuCorts läkemedelskandidat utföll långsammare i relation till referensprodukten.
Efter studieresultaten blev kända har AcuCort tillsatt en expertgrupp för att utreda följande punkter:
- Orsaken till utfallet.
- Presentera handlingsalternativ för att möjliggöra fortsatt registrering av ISICORT® i USA.
- Utvärdera konsekvenserna av de olika handlingsalternativen.
Hittills har möjliga orsaker till utfallet identifierats och arbetet att utvärdera dessa pågår.
Gällande eventuella konsekvenser för marknadsgodkännande i Sverige blir dessa inte kända innan Läkemedelsverket inkommer med frågor till AcuCort, vilket förväntas ske som tidigast under första kvartalet nästa år.
“AcuCorts målsättning att registrera och kommersialisera ISICORT® ligger fortsatt fast. Vi har stort förtroende för expertgruppen och kommer att informera om status i takt med att arbetet går framåt”, säger Mats Lindfors, VD för AcuCort.
Denna nyhet innehåller inga konkreta besked vad nästa steg kommer vara eller hur tidsplan och kostnader påverkas av att inte uppnå bioekvivalens. Det är däremot positivt att marknaden får besked om vilka delar som inte uppnådde bioekvivalens och att bolaget arbetar med att utforma en konkret plan för vägen framåt.
Det finns exempel på andra bolag vars produkt först inte uppnått bioekvivalens men som efter justeringar har lyckats korrigera de variabler som skilde sig mot referensprodukten. Exempelvis lyckades Enorama Pharma uppnå bioekvivalens på cirka två månader efter en studie där de inte uppnådde bioekvivalens. Givetvis har AcuCort en helt annan produkt och det är möjligt att Enorama Pharmas nikotintuggummi skilde sig relativt lite mot referensprodukten från början och därför lyckades göra snabba justeringar. Innan vidare besked ges från AcuCort går det inte att spekulera gällande tidsplan för ny bioekvivalensstudie men det kan konstateras att det är möjligt att göra justeringar för att korrigera de variabler som skiljer sig mot referensprodukten.
AcuCorts läkemedelskandidat ISICORT® uppnådde ej krav på bioekvivalens i USA
2019-10-16
Igår den 15 oktober 2019 presenterade AcuCort resultat från den andra av två bioekvivalensstudier för registrering av läkemedelskandidaten ISICORT®.
Bioekvivalensstudien gjordes på icke-fastande deltagare och i jämförelse med en redan godkänd referensprodukt, där ISICORT® uppnådde bioekvivalens i två av tre kriterier. Eftersom värdet inte hamnade inom godkända intervall för alla tre kriterier så uppnåddes inte heller tillräcklig bioekvivalens för registrering i USA.
Tidigare har AcuCort utfört bioekvivalensstudier på fastande deltagare för registrering i USA och då uppnåddes bioekvivalens. Enligt Analyst Groups bedömning är det troligt att detta kommer påverka kostnadsbilden och tidsplanen för marknadsgodkännande i USA, men det är inget som bolaget ännu har uttalat sig om. AcuCort kommer fortsatt arbeta mot kommersialisering i USA och kommer tillsammans med relevanta experter utvärdera vilka handlingsalternativ som är bäst i dagens situation.
Resultatet från bioekvivalensstudien på icke-fastande deltagare kommer inte ha någon påverkan för ansökan om marknadsgodkännande i Sverige, och vidare EU, eftersom det i detta fall enbart krävs bioekvivalensstudie på fastande deltagare. Den genomförda bioekvivalensstudien på fastande deltagare ligger till grund för den inskickade ansökan om marknadsgodkännande i Sverige.
Analyst Group har ställt några korta frågor till VD Mats Lindfors.
Vad innebär det att bioekvivalens inte har uppnåtts för ansökan i USA?
Vi har uppnått bioekvivalens med fastande deltagare, men inte med icke-fastande. Vi kommer att undersöka såväl konsekvenser som möjliga handlingsvägar framåt.
Vilka steg kommer ni ta för att uppfylla de amerikanska kriterierna?
Det är idag för tidigt att kommentera. Vi har nu kommunicerat resultatet och som jag nämner i PM:et så behöver vi, givetvis tillsammans med relevanta experter, analysera och undersöka och värdera vilka möjligheter som erbjuds för att ta ISICORT vidare mot registrering och kommersialisering.
Kommer detta signifikant påverka tidsplanen för godkännande i USA?
Det är för tidigt att kommentera.
Hur stora kostnader kan väntas som konsekvens av att inte uppnå bioekvivalens?
Det är för tidigt att kommentera.
Kommer detta ha någon påverkan på ansökan om marknadsgodkännande i Sverige?
Sverige och EU kräver inte studier med icke-fastande deltagare för godkännande. Det är dock för tidigt att förutspå eventuell påverkan av utfallet från USA studien på den svenska ansökan.
Läs mer om AcuCort här
AcuCort justerar strategin för ansökan om marknadsgodkännande av ISICORT® inom EU
2019-09-05
AcuCort har presenterat en justering av strategin för ansökan om marknadsgodkännande av ISICORT® inom EU.
Justeringen av strategin innebär att registreringsprocessen börjar med en nationell hybridansökan i Sverige, för att sedan följas av en ansökan för fler EU-länder via Mutual Recognition Processen (MRP), givet godkännande i Sverige. Syftet med justeringen är enligt AcuCort att snabbt och säkert nå ett godkännande av läkemedelskandidaten ISICORT® brett inom EU.
Det finns flera regulatoriska vägar mot att nå godkännande inom EU och tillsammans med den regulatoriska partnern ProPharma Group har bolaget utvärderat olika alternativ sett till risker, tidsplaner och kostnader. Vid övervägning av dessa faktorer är slutsatsen att AcuCort kommer justera strategin till en hybridansökan som startar i Sverige och fortsätts genom MRP vid godkännande i Sverige. Tidigare var strategin att genomföra en hybridansökan i en så kallad Decentraliserad Process (DCP), som innebär att ett referensland utvärderar ansökan om godkännande för flera länder i ett och samma steg. Detta valdes bort i samråd med ProPharma Group eftersom risken att ansökan skulle bli mer tidskrävande, på grund av förhandlingar med fler länder samtidigt, ansågs vara större.
Det första steget i processen väntas inledas under de närmaste veckorna genom att en nationell hybridansökan lämnas in i Sverige. Jämfört med tidigare strategi förväntar sig AcuCort ingen väsentlig kostnadsförändring i och med den justerade strategin.
“Jag är övertygad om att två-stegslösningen representerar det bästa regulatoriska vägvalet för AcuCort och jag ser med tillförsikt framemot den fortsatta vägen mot kommersialisering av ISICORT®”, säger Mats Lindfors, VD på AcuCort.
Analyst Group bedömer nyheten som positiv, då beslutet att justera strategin visar att samarbetet med regulatoriska partners är fruktsamt och att arbetet mot läkemedelsgodkännande underlättas av extern kompetens. Förhoppningsvis innebär den uppdaterade strategin att ISICORT® blir godkänt snabbare och att kommersialiseringen inom EU sker tidigare än förväntat.
AcuCort genomför emission
2019-08-29
AcuCort presenterade den 27 augusti en företrädesemission vilken vid full teckning tillför AcuCort 41,2 MSEK, före emissionskostnader.
Bakgrunden till nyemissionen är att bolaget behöver kapital för att fortsätta arbetet mot kommersialisering av läkemedelskandidaten ISICORT®. AcuCorts produkt ISICORT® är ett läkemedel mot svåra och akuta allergiska reaktioner, i form av en tunn film som upplöses på patientens tunga. För att nå kommersialisering behöver AcuCort genomföra den pågående bioekvivalensstudien med positiva resultat, få läkemedelsgodkännande från EU och amerikanska myndigheter, sluta avtal med kommersiella partners för distribution och/eller licensiering samt utveckla varumärket ISICORT®. Denna process är kapitalintensiv och därför genomför AcuCort nu en nyemission.
Information om nyemissionen
- Avstämningsdagen är den 3:e september.
- Teckningsperiod mellan 6-20 september.
- För varje befintlig aktie på avstämningsdagen har aktieägare företrädesrätt att teckna en ny aktie.
Fördelning av emissionslivkvid
- Regulatoriska processer; 35 procent
- Försäljning och marknadsföringsaktiviteter; 10 procent
- Förstärkning av rörelsekapital; 17 procent
- Immateriella rättigheter; 5 procent
- Företagsledning och administration; 25 procent
- Farmakovigilans; 8 procent
Regulatoriska processer samt företagsledning och administration är de största posterna, vilka är hänförliga till processen att få ett beviljat läkemedels- och marknadsgodkännande samt kostnader för övriga steg som måste tas för att nå kommersialisering.
Storleken på emissionen var större än vad vi förväntat. Trots att detta innebär större utspädning än väntat för aktieägares befintliga innehav, innebär också storleken på nyemissionen att bolaget står på stabilare finansiella grunder inför kommersialisering. Detta reducerar osäkerheten kring AcuCorts finansiella ställning framgent och ger bolaget möjlighet att fokusera på kommersialiseringen.
Kort intervju med VD Mats Lindfors
AcuCort genomför nu en emission om ca 41 MSEK före emissionskostnader – bedömer ni att denna kommer bli den sista kapitalanskaffningen bolaget gör innan ni når break-even?
Villkorat att emissionen fulltecknas, och att vi uppnår våra mål i affärsplanen så är det mycket möjligt att detta är den sista kapitalanskaffningen.
Finns det någon uppdatering kring den tidigare kommunicerade tidsplanen att vänta?
Vi kommer att kommunicera uppdateringar när det finns ny pålitlig data tillgänglig.
Kan du berätta lite mer om vad som innefattar”företagsledning och administration” gällande er allokering av emissionslikviden?
Personal d.v.s. anställda inkl. utbyggnad av organisationen samt styrelse och vissa konsulter är den dominerande delen. Kostnader för att bygga upp ett kvalitetssystem i samband med att bolaget blir innehavare av marknadstillstånd är en annan viktig del, likaså kostnader för att införa så kallad serialisering i produktionen. Serialisering är en kvalitetssäkringsåtgärd för att kunna spåra produkter ner på förpackningsnivå.
AcuCort presenterade idag sin kvartalsrapport för det andra kvartalet 2019
2019-08-16
I rapporten noteras inga väsentliga överraskningar, även om rörelseresultatet var cirka 1 MSEK lägre än estimerat som följd av något högre övriga externa kostnader. Kostnadsökningen i jämförelse med det första kvartalet bedöms bero på utgifter relaterade till godkännandeprocessen för Dexa ODF i EU och USA.
Under det andra kvartalet har AcuCort valt Öhrlings PricewaterhouseCoopers AB som revisionsbolag, vilket har inneburit förändringar i den historiska redovisningen av immateriella tillgångar för åren 2012 och 2013. Detta har emellertid inte fått några konsekvenser för bolagets rörelse, resultat eller kassaflöde. Framgent kommer AcuCort redovisa aktiverat arbete för egen räkning uppdelat på varje kvartal, istället för enbart i det fjärde kvartalet som tidigare varit fallet.
I VD-ordet från Mats Lindfors framgår det att Bolaget har gjort fortsatta framsteg. AcuCorts regulatoriska partner, Sofus ProPharma, arbetar intensivt med sammanställningen av ansökan för godkännande av Dexa ODF i EU. Vidare har Bolaget fått klartecken att påbörja den andra bioekvivalensstudien i USA som kommer ske med icke-fastande deltagare, detta efter ett positivt resultat från den första studien. Lindfors kommenterar också beskedet från det europeiska patentverket att godkänna patentansökan för ”Dexamethasone ODF” och menar att patentet stärker Bolagets förhandlingsposition i diskussioner med potentiella kommersiella partners.
Vid en extra bolagsstämma i juni gavs styrelsen bemyndigande att besluta om nyemission vid ett eller flera tillfällen innan nästa årsstämma. AcuCort förväntas genomföra en nyemission under det andra halvåret 2019, i syfte att finansiera den fortsatta processen att nå kommersialisering. Med utgångspunkt i att Bolagets kostnader fortlöper i ungefär samma takt som under det första halvåret kommer ett kapitaltillskott vara nödvändigt innan årsskiftet. Dagens rapport innehöll däremot inte vidare information om när nyemissionen väntas presenteras.
Rörelseresultatet för det andra kvartalet blev -2,2 MSEK, vilket var lägre än väntat som följd av högre övriga externa kostnader. Detta kan jämföras med -1,4 MSEK under första kvartalet (Q1-19). En möjlig förklaring till de högre kostnaderna är en intensifiering av processerna kring läkemedelsgodkännande, vilket bl.a. medför kostnader för konsulter m.m. Analyst Group kommer inför analysuppdateringen undersöka detta vidare.

Vi kommer inom kort att återkomma med en uppdaterad aktieanalys
AcuCort publicerar imorgon sin Q2-rapport
2019-08-15
Imorgon den 16 augusti publicerar AcuCort sin delårsrapport för andra kvartalet 2019, följande är våra tankar inför rapporten.
Fortsatt arbete för att nå kommersialisering av Dexa ODF
Under kvartalet har AcuCort fortsatt ta steg mot marknadsgodkännande och kommersialisering av läkemedlet Dexa ODF, detta har exempelvis mynnat ut i ett myndighetsgodkännande efter det andra kvartalets utgång att genomföra den återstående bioekvivalensstudien i USA. Studien är av stor betydelse för AcuCort eftersom den är avgörande för godkännande för försäljning i USA. Bioekvivalensstudien kommer kunna starta redan under tredje kvartalet 2019. Vidare har Bolaget fortsatt fört samtal med potentiella partners och det bedöms vara avgörande för en lyckad kommersialisering att AcuCort hittar en eller flera lämpliga partners för licensiering eller distribution.
De finansiella räkenskaperna för det andra kvartalet väntas inte innehålla några större överraskningar, utan till stor del vara lik föregående kvartal. Vi kommer först och främst titta närmare på rörelsekostnaderna, vilka estimeras uppgå till ca -1,4 MSEK. Aktiverat arbete för egen räkning estimeras kring 0,25 MSEK, vilket ger ett förväntat rörelseresultat om ca -1,15 MSEK. Inga kommunicerade händelser har skett under kvartalet som bedöms ha påverkat rörelsekostnaderna till en betydande grad.
Under kvartalet har AcuCort valt Öhrlings PricewaterhouseCoopers som revisionsbolag, vilket har lett till vissa förändringar i redovisningen. Framgent kommer AcuCort redovisa aktiverat arbete för egen räkning för varje kvartal, istället för en gång per år under det fjärde kvartalet. Det innebär att rörelseresultatet, likt under Q2-19, även för resterande kvartal kommer att öka.
Fokus på utveckling inom läkemedelsgodkännande, partnersamtal och kapitalbehov
De faktorer som investerare bör fokusera på i kvartalsrapporten och tillhörande VD-ord är enligt Analyst Groups bedömning följande:
- Läkemedelsgodkännande. Kommande kvartal väntas fortsatta bioekvivalensstudier för eventuellt godkännande av Dexa ODF i USA. Även uppdateringar om produktgodkännandeprocessen i EU, där AcuCort samarbetar med Sofus Regulatory Affairs, är viktiga att följa.
- Partnersamtal. För att nå kommersialisering av Dexa ODF väntas Bolaget behöva ingå samarbete med partners för distribution och/eller licensiering. Inga konkreta samarbetspartners är kända, men enligt föregående VD-ord förs diskussioner med flera aktörer.
- Kapitalbehov. Det fortsatta utvecklingsarbetet, diverse förberedelser för kommersialisering, samt ansökningsprocesser väntas kräva en nyemission under andra halvåret 2019.
Vi kommer att återkomma med en uppdaterad aktieanalys efter rapporten.
Uppföljning på AcuCorts Q1-19
2019-05-17
AcuCort (“AcuCort” eller “Bolaget”) publicerade idag den 17 maj sin delårsrapport för Q1-19. Nedan följer Analyst Groups tankar om rapporten.
I rapporten syns inga större överraskningar, med undantaget att Bolagets burn rate var lägre än väntat, vilket är positivt. Trots hög aktivitet under kvartalet på det regulatoriska planet lyckas Bolaget hålla nere kostnaderna, vilket är positivt inför framtida stundande nyemission.
I VD Mats Lindfors VD-ord framgår att mycket positivt har hänt kring Bolaget under kvartalet. Vidare framgår även att AcuCort har upplevt ett stort intresse för Dexa ODF under Bio-Europe-konferensen i Wien, som ägde rum mot slutet av mars. Tack vare läkemedlets regulatoriska framsteg har intresset för Dexa ODF ökat, och flertalet sekretessavtal angående samtal kring potentiellt samarbete har skrivits på. Detta är en väsentlig del för Bolagets framtid, och en av de viktigaste delarna att följa i AcuCorts framtida utveckling. Därav är det helt klart positivt med ett så stort intresse för produkten.
Vad gäller Bolagets finansiella utveckling under kvartalet lyckades AcuCort hålla nere kostnaderna, och levererade ett bättre resultat än väntat. Trots hög aktivitetsnivå levererar Bolaget en EBIT på -1,37 MSEK. Detta är en något förbättrad siffra till följd av att Bolaget aktiverar utgifter till balansräkningen, vilket förbättrar resultatet men förstorar balansräkningen. Justerat för detta, om Bolaget hade kostnadsfört samtliga kostnader, hade EBIT rapporterats till -2,38 MSEK. Trots detta är det fortfarande en lägre siffra än vad vi förväntade, och att Bolaget lyckas leverera en så låg kostnadsnivå är positivt. Bolagets burn rate låg på -2,7 MSEK. Sammantaget bedöms rapporten vara ett styrkebesked på alla fronter, där Bolagets låga kostnadsnivå samt att ett antal sekretessavtal med potentiella partners har slutits indikerar en positiv framtid för AcuCort.

Analyst Group kommer återkomma med en uppdaterad analys inom kort.
Kommentar inför AcuCorts Q1-19
2019-05-16
AcuCort (“AcuCort” eller “Bolaget”) publicerar imorgon sin delårsrapport för Q1-19. Följande är Analyst Groups tankar inför rapporten.
AcuCorts första kvartal har präglats av flertalet händelser, med en godkänd bioekvivalensstudie i EU och en av två bioekvivalensstudier godkända i USA. Vidare har även Bolaget börjat genomföra den andra studien i USA, vilket väntas ge svar inom en snar framtid.
Bolaget har även anlitat Sofus Regulatory Affairs, en konsult inom regulatoriska ärenden som kommer hjälpa Bolaget att sammanställa sin ansökan för läkemedelsgodkännande inom EU.
Det är mycket som har hänt kring AcuCort under det senaste kvartalet som har påverkat värdet på Bolaget, och det kommer bli intressant att läsa hur VD Mats Lindfors uttalar sig om framtiden samt om han har någon kommentar på hur den andra bioekvivalensstudien i USA går.
Främst kommer fokus ligga på Bolagets burn rate under kvartalet, där kassan är högst intressant att följa i och med den kommunicerade nyemissionen som stundar under 2019. Denna kommer vara högst relevant för framtiden, och trots att den är kommunicerad verkar marknaden visa upp en osäkerhet kring just denna och därav kommer det bli intressant att se om Bolaget nämner något om en plan för detta i morgondagens rapport.
Vidare vill vi se se hur Bolagets fortsatta arbete med att hitta potentiella samarbetspartners för Dexa ODF går. Detta bedöms vara den största risken i Bolaget förutom den läkemedelsspecifika risken, och blir därför intressant att följa.
Avslutningsvis väntas rapporten vara en rapport som egentligen inte bjuder på några större överraskningar. Kostnadsmassan bedöms ligga på en relativt hög nivå till följd av Bolagets höga aktivitet under kvartalet. Detta är en effekt av att AcuCort fortsätter sitt arbete mot marknadslansering, och visar på Bolagets fortsatta framfart.

Acucort senarelägger ansökan om produktgodkännande
2019-03-18
AcuCort (“AcuCort eller “”Bolaget”) meddelade igår om att studieansökan för läkemedelsgodkännande i EU kommer att förskjutas.
Förskjutningen blir från Q2-19 till Q3-19. Detta till följd av att produkten som Bolaget ansöker med måste klara av att bevaras under en 12-månadersperiod under specifika förhållanden för att kunna användas som ansökningsobjekt, detta enligt regulatoriska skäl.
Förskjutningen kommer inte att påverka Bolagets verksamhet väsentligt, då det inte har något med produktens egenskaper att göra, utan endast att uppfattningen hos Bolaget tidigare har varit att det räckte med att förvara produkten i en 6-månadersperiod. Detta kommer dock innebära att den planerade lanseringen av produkten kommer skjutas upp. Försäljningsstarten av produkten är att anse som en väsentlig potentiell trigger för aktiekursen, något som nu skjuts upp. Samtidigt finns det andra tydliga triggers i Bolagets närtid, främst ett samarbetsavtal, som ligger närmast som den mest aktuella, något som är en väsentlig del på vägen mot marknadslansering. Sammanfattningsvis påverkar inte gårdagens PM verksamheten i en större utsträckning då det inte påverkar storleken på de framtida kassaflödena, och är inte heller någon grav försening av den tidigare publicerade tidsplanen.
Vidare kommer det även bli intressant att se VD Mats Lindfors presentation under dagen för att se hur verksamheten går och hur AcuCort ser på framtiden.
Analytikerkommentar på AcuCorts delårsrapport för Q4-18
2019-02-19
AcuCort (“AcuCort” eller “Bolaget”) publicerade den 23 januari sin delårsrapport för Q3-18. Nedan är vår sammanfattning av rapporten samt hur vi ser på AcuCort framgent.
Status 2019
Under de senaste månaderna har det hänt många intressanta skeden kring AcuCort, och Bolaget har tagit stora steg fram mot marknadsgodkännande och kommersialisering av Dexa ODF. Bolaget har under den senaste perioden fått en godkänd bioekvivalensstudie i EU, börjat genomföra sin bioekvivalensstudie i USA samt anlitat konsulten SOFUS Regulatory Affair, för att färdigställa Bolagets ansökan om läkemedelsgodkännande i EU.
Chanserna för ett positivt utfall bedömdes till 70 % innan resultatet publicerades. Bolaget har sedan tidigare genomfört en studie som var snarlik den som precis utförts, med den enda stora skillnaden att tillverkningen utfördes av ett annat bolag. Adhex Pharma, det bolag som AcuCort nu använder sig av väntas leverera de filmer som kommer att användas för Bolagets studier för ett godkännande i USA och Asien, vilket är en av anledningarna till att risken för dessa nu bedöms vara betydligt lägre än tidigare.
Att den läkemedelsspecifika risken i Bolaget sjunker påverkar värderingen
Tidigare bedömdes en sannolikhet för godkännande till 70 %. I och med den godkända studien skapas nu en ojämnt fördelad risk mellan de olika geografiska marknaderna. I EU är risken inte utraderad, men mycket talar för att att läkemedlet blir godkänt högt, då endast en läkemedelsansökan kvarstår. I de övriga primära marknaderna, Asien och Nordamerika, bedöms även risken nu vara lägre än tidigare.
Att AcuCort har visat på att läkemedlet håller en hög standard med tillverkaren Adhex Pharma i och med bioekvivalensstudien, bidrar till att chansen för att godkännande i dessa områden blir högre. Sammantaget kommer dessa faktorer påverka värderingen av AcuCort positivt.
Vad som nu väntar är ett större fokus på hur AcuCorts arbete med potentiella samarbetspartners fortgår. Bolaget börjar närma sig ett läkemedelsgodkännande inom EU som beräknas ske mot slutet av 2019, och en påbörjad försäljning under 2020. För att möjliggöra detta krävs ett gediget arbete för att lyckas nå avtal med så kompetenta partners som möjligt.
VD Mats Lindfors har under hösten arbetat hårt mot detta mål, Mats medverkade på en stor läkemedelskonferens i Köpenhamn under november, och har kommunicerat att han för samtal med ett antal intressanta aktörer. Han kommer även fortsätta med detta arbete under 2019, och med tanke på de patientfördelar som Dexa ODF kan påvisa, väntas det finnas ett stort intresse för produkten finnas hos potentiella partner, och därav väntas Bolaget lyckas sluta ett avtal.
Kommentar på bokslutskommunikén
AcuCorts Q4 kom inte med några överraskningar. Bolaget fortsätter sitt arbete enligt tidsplan som tidigare kommunicerats, och inget oväntat presenterade sig i rapporten. Bolaget kommunicerade att en nyemission är att vänta under den kommande 12-månaderspersioden, vilket är något som tidigare kommunicerades i samband med den tidigare emissionen, och är därav inget oväntat besked. I övrigt syns inga egentliga överraskningar i rapporten, Bolaget fortsätter med sitt arbete och Analyst Group går in i 2019 med positiv inställning till AcuCort och utvecklingen av Dexa ODF.
Sammantaget finns det anledning att vara positiv till AcuCorts verksamhetsutveckling framgent.
Analyst Group kommer att återkomma med en uppdaterad aktieanalys inom snar framtid.
Analytikerkommentar på AcuCorts delårsrapport Q3-18
2018-11-07
AcuCort AB (”AcuCort” eller ”Bolaget”) publicerade idag den 7 november sin delårsrapport för tredje kvartalet 2018. Nedan framgår våra tankar om rapporten.
Dexa ODF-studier går enligt tidsplan
Under det andra halvåret 2018 har AcuCort inlett studier med hjälp av Quinta-Analytica, som sedan skall användas som underlag för ansökningar om läkemedelsgodkännande i EU och USA. Att få en statusuppdatering angående hur denna process har utvecklat sig hittills var därför den punkten Analyst Group fokuserade på mest innan rapport. I rapporten kan vi utläsa i Mats Lindfors VD-ord att dessa studier går enligt tidsplan. Vi kan luta oss mot historien och se att Bolaget hittills har hållit vad de har lovat inom uttalad tidsplan när sådana uttalanden tidigare gjorts. Därav drar Analyst Group slutsatsen att detta är ett positivt uttalande av Mats, och är fortsatt positiva till hur studiens utfall blir.
Vidare såg vi att kostnadsmassan var högre än förväntat. Det är möjlig att denna kostnad är hänförlig till Bolagets möte med FDA. Läkemedelsprocessen inom USA prognostiseras vara den mest kostsamma av alla regioner Bolaget kommer söka till, och därav ses detta som en logisk förklaring till att kostnaderna inte låg i linje med Analyst Groups estimat. Vidare väntas kostnadsmassan vara fortsatt hög under Q4-18, till följd av att majoriteten av kostnaderna relaterade till Quinta-Analyticas studie av Dexa ODF väntas bokas in under denna period.
Analyst Group anser att Q3-rapporten var bra, kostnadsöverraskningen till trots. Här låg dock inte fokus inför rapporten, utan det vi såg mest fram emot var VD-ordet och kommentar kring hur studien av Dexa ODF har utvecklats. AcuCort gav bra information kring detta och Analyst Group är fortsatt positiva till Bolagets framtid. AcuCort går nu in i en spännande fas med där flera potentiella värdedrivare kan inträffa, t.ex. positiva studieresultat eller påskrivet samarbetsavtal med en partner. Det kan komma att driva på värderingen av Bolaget och aktien.
Analytikerkommentar inför AcuCorts delårsrapport för Q3-18
2018-11-06
AcuCort AB (”AcuCort” eller ”Bolaget”) publicerar imorgon den 7 november sin delårsrapport för tredje kvartalet 2018. Följande är våra tankar inför rapporten.
Den senaste perioden för AcuCort har varit händelserik. Bolaget har under de senaste månaderna slutfört produktionen av de exemplar av Dexa ODF som används under Bolagets studier, genomfört en övertecknad företrädesemission om 10,8 MSEK (efter emissionskostnader), haft ett möte med FDA angående ansökningsprocessen för läkemedelsgodkännande.
I rapporten ser vi fram emot att läsa om en statusuppdatering angående hur AcuCorts studier fortskrider. Studierna har påbörjats, och beroende på status kan detta ses som en potentiell trigger.
Vidare blir det även intressant att titta på hur Bolaget hanterar kostnaderna. Rörelsekostnaderna väntas sjunka kraftigt jämfört med Q2 2018. Detta till följd av att majoriteten av kostnaderna då bestod av kostnader relaterade till Adhex Pharma. Under Q3-18 väntas Bolagets kostnadsmassa ha återgått till mer normala nivåer. Extraordinära kostnader under kvartalet väntas främst vara relaterade till Quinta-Analytica, alltså den pågående studien. I samband med nyligen genomförd nyemission guidade Bolaget för hur stor kostnadsmassan kommer att vara för studien. Frågan är hur stor del av denna kostnad som bokats under Q3-18. Analyst Group estimerar att ca 20 % av denna summa, cirka 400 tSEK kommer bokas under Q3-18.
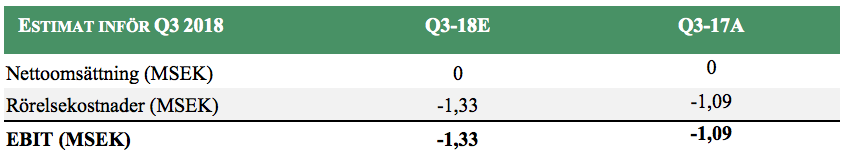
Sep
Intervju med AcuCorts VD Mats Lindfors
Nov
Aktieanalys på AcuCort Q3-18
Share price
0.74
Valuation Range
2022-03-07
Bear
2,0 SEKBase
4,4 SEKBull
6,6 SEKDevelopment
Principal shareholder
2021-09-30



Kommentar på AcuCorts Q1-rapport
2021-04-29
AcuCort publicerade igår den 28 april 2021 sin delårsrapport för första kvartalet 2021. Följande är vår uppföljning av rapporten och vad vi främst fokuserat på.
Precis som vi skrivit tidigare bedriver AcuCort fortfarande ett utvecklingsarbete, parallellt med att förberedelserna för den kommersiella fasen fortlöper, varför ingen försäljning är aktuell i dagsläget. Det, i kombination med nödvändiga investeringar och rörelsekostnader, resulterar i ett negativt kassaflöde. Med tanke på vad för typ av bolag AcuCort är och vart de just nu befinner sig i sin utvecklingsfas, är det inget konstigt, samtidigt som det fortsatt är viktigt att effektivt nyttja den likviditeten som finns i bolaget. Vid utgången av första kvartalet uppgick kassan till ca 21,6 MSEK, vilket kan jämföras med ca 24 MSEK vid utgången av december (Q4-20). Under första kvartalet 2021 uppgick därmed bolagets kapitalförbrukning, s.k. burn rate, till -0,8 MSEK/månad, vilket är i linje med genomsnittet för 2020 och således fortsatt lågt. Vi ser såklart positivt på detta, samtidigt som vi dock under kommande kvartal fortsatt räknar med att AcuCort kommer ha en något högre kapitalförbrukning, vilket är helt naturligt med tanke på den kommande kommersialiseringen. Med det sagt, och med tanke på den utgående kassan per den sista mars, anser vi fortsatt att AcuCort har en mycket stark finansiell position.
Under årets första kvartal uppgick AcuCorts totala rörelsekostnader till ca -2,0 MSEK, att jämföra med ca -2,7 MSEK under Q1-20 och -1,9 MSEK under Q4-20. AcuCort utvecklas således fortsatt med en god kostnadskontroll, vilket i sin tur bidragit till den ovannämnda låga kapitalförbrukningen som bolaget uppvisar.
Under våren har AcuCort anställt Louise Harting som projektledare, Louise har en masterexamen i International Business från Copenhagen Business School, och erfarenhet av internationella produktlanseringar inom läkemedelsindustrin från bl.a. Novo Nordisk. I sin roll som projektledare på AcuCort har hon ansvaret för bl.a. ansökningarna om marknadsregistrering av ISICORT® i Norden och Europa. AcuCort fortsätter därmed att addera viktiga pusselbitar för att accelerera utvecklingen i bolaget och öka chanserna för en lyckad marknadsintroduktion av ISICORT®.
Det stora fokuset framgent är hänförligt till just arbetet med att lansera ISICORT® på marknaden vilket inkluderar att allt ska komma på plats så effektivt som möjligt enligt den fastställda planen för att säkerställa en storskalig kommersiell produktion. Det innebär exempelvis att valideringsbatcher och labbanalyser granskas, liksom att kvalitetsparametrar och analyser kontrolleras och följs upp. Parallellt med detta fortsätter de aktiva dialogerna med olika potentiella licenstagare och samarbetspartners. Eventuell kommunikation kring detta, vilket Analyst Group ser som tänkbart under kommande kvartal i år, kan komma att utgöra en stark värdedrivare i aktien. Med det i åtanke, och med hänsyn till nuvarande bolagsvärde om ca 90 MSEK i skrivande stund, ser vi en fortsatt attraktiv risk-reward i aktien.
Vi kommer att återkomma med en uppdaterad version av vår senaste aktieanalys.